Bravais -Netzwerkkonzept, Merkmale, Beispiele, Übungen
- 4852
- 42
- Frederike Birkemeyer
Der Bravais -Netzwerke Sie sind der Satz von vierzehn dreidimensionalen Einheitenzellen, in denen die Atome eines Kristalls. Diese Zellen bestehen aus einer dreidimensionalen Anordnung von Punkten, die eine Grundstruktur bilden, die in den drei räumlichen Richtungen regelmäßig wiederholt wird.
Der Ursprung dieser Konfession für grundlegende kristalline Strukturen stammt aus dem Jahr 1850, als Auguste Bravais zeigte, dass nur 14 mögliche grundlegende dreidimensionale Einheitszellen möglich sind.
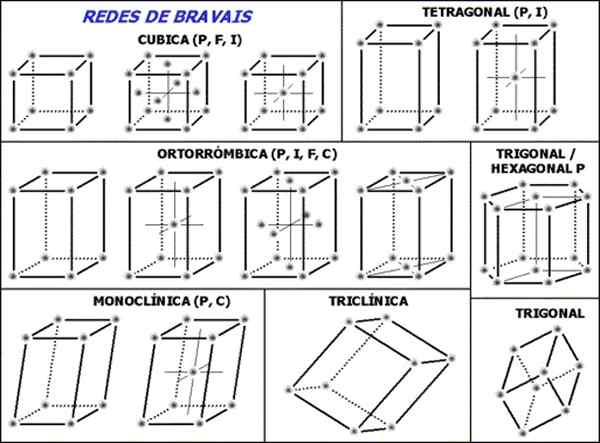
 Abbildung 1. Bravais -Netzwerke sind der Satz der 14 notwendigen und genügend Einheitszellen, um eine kristalline Struktur zu beschreiben. (Wikimedia Commons)
Abbildung 1. Bravais -Netzwerke sind der Satz der 14 notwendigen und genügend Einheitszellen, um eine kristalline Struktur zu beschreiben. (Wikimedia Commons) Der Satz der 14 Bravais -Netzwerke wird gemäß der Geometrie der Zellen in sieben Gruppen oder Strukturen unterteilt. Diese sieben Gruppen sind:
1- kubisch
2- teretragonal
3-ortorrombisch
4-trigonal-hexagonal
5- monoklin
6-Triklin
7-Trigonal
Jede dieser Struktur definiert eine einheitliche Zelle, dies ist der kleinste Teil, der die geometrische Anordnung von Atomen im Glas behält.
[TOC]
Eigenschaften von Bravais -Netzwerken
Die vierzehn Netze Bravais sind, wie oben angegeben, in sieben Gruppen unterteilt. Jede dieser Gruppen hat jedoch ihre Einheitszellen mit ihren charakteristischen Parametern, die sind:
1- Der Netzwerkparameter (a, b, c)
2- Anzahl der Atome pro Zelle
3- Beziehung zwischen Netzwerkparameter und Atomradio
4- Koordinationsnummer
5- Verpackungsfaktor
6- Interstitielle Räume
7- Durch Übersetzungen entlang der Vektoren A, B, C Die kristalline Struktur wird wiederholt.
Kubiknetzwerke
Es besteht aus dem einfachen oder kubischen kubischen Netzwerk, dem kubischen Netzwerk, das sich auf Gesichter oder Kubiknetzwerk f und das kubische Netzwerk auf der Kubikbehörde oder des Kubikkörpers oder des Netzwerks konzentriert.
Alle kubischen Netzwerke haben die drei Netzwerkparameter Entsprechend den x, y -Adressen, z mit demselben Wert:
A = b = c
Kubiknetzwerk p
Es ist zweckmäßig hervorzuheben, dass Atome durch Kugeln dargestellt werden, deren Zentren in den Eckpunkten der Kubikzelle p sind.
Kann Ihnen dienen: künstliche SatellitenIm Falle des Kubiknetzwerks p die Anzahl der Atome pro Zelle Es ist 1, denn in jedem Scheitelpunkt befindet sich nur der achte Teil des Atoms in der Einheitszelle, dann 8*⅛ = 1.
Er Koordinationsnummer Zeigt die Anzahl der Atome an, die in der Nähe Nachbarn im kristallinen Netzwerk sind. Im Falle des Kubiknetzes P beträgt die Koordinationsnummer 6.
Kubiknetzwerk i
In dieser Art von Netzwerk zusätzlich zu den Atomen in den Eckpunkten des Würfels befindet sich ein Atom in der Mitte des Würfels. So Atomzahl pro Zelle Einheitlich im Kubiknetzwerk P beträgt 2 Atome.
 Figur 2. Körpergeräte kubisches Netzwerk.
Figur 2. Körpergeräte kubisches Netzwerk. Kubiknetzwerk f
Es ist das kubische Netzwerk, das zusätzlich zu den Atomen in den Eckpunkten ein Atom in der Mitte des Gesichts jedes Würfels hat. Er Anzahl der Atome pro Zelle Es ist 4, da jedes von sechs Atomen des Gesichts die Hälfte in der Zelle hat, dass 6*½ = 3 plus 8*⅛ = 1 in den Scheitelpunkten.
 Figur 3. Kubiknetzwerk konzentriert sich auf Gesichter.
Figur 3. Kubiknetzwerk konzentriert sich auf Gesichter. Sechseckalales Netzwerk
In diesem Fall ist die Einheitszelle ein gerade sechseckiger Prisma. Sechseckige Netzwerke haben die drei Netzwerkparameter Entsprechende Erfüllung der folgenden Beziehung:
A = b ≠ c
Der Winkel zwischen Vektor A und B von 120 ° ist, wie in der Abbildung gezeigt. Während zwischen den Vektoren A und C sowie zwischen B und C sind gerade Winkel.
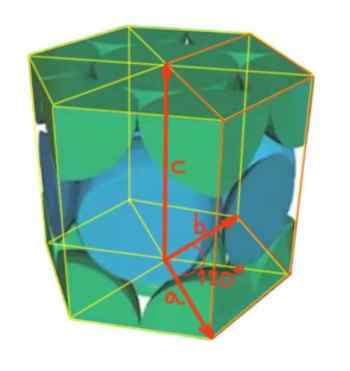 Figur 4. Sechseckalales Netzwerk.
Figur 4. Sechseckalales Netzwerk. Er Anzahl der Atome pro Zelle Es wird wie folgt berechnet:
- In jeder der 2 Basen des sechseckigen Prismas gibt es 6 Atome in den sechs Eckpunkten. Jedes dieser Atome nimmt ⅙ der einheitlichen Zelle ein.
- In der Mitte jedes der 2 hexagonalen Basen befindet sich 1 Atom, das 1/2 einheitliche Zelle einnimmt.
- Auf den 6 lateralen Gesichtern des hexagonalen Prismas gibt es jeweils 3 Atome, von denen jeweils ⅔ der Einheitszelle einnimmt, und 3 Atome, die jedes Volumen der Einheitszelle einnehmen.
Es kann Ihnen dienen: Kraft hören: Oberflächen- und Massenkräfte(6 x ⅙) x 2 + ½ x 2 + ⅔ x 3 + ⅓ x 3 = 6
Die Beziehung zwischen den Netzwerkparametern A und B mit dem Atomradius R unter der Annahme, dass alle Atome von gleichem Funk sind und in Kontakt stehen, lautet:
a/r = b/r = 2
Beispiele
Metalle sind die Hauptbeispiele für kristalline Strukturen und auch die einfachsten, da sie im Allgemeinen aus einer einzelnen Atomart bestehen. Aber es gibt andere nicht -metallische Verbindungen, die auch kristalline Strukturen wie Diamant, Quarz und viele andere bilden.
- Das Bügeleisen
Eisen hat eine einfache Kubikeinheitszelle mit Netzwerkparameter oder Kante A = 0,297 nm. In 1 mm gibt es 3,48 x 10^6 Einheitszellen.
- Kupfer
Es hat eine kubische kristalline Struktur, die auf Gesichtern zentriert ist und nur durch Kupferatome gebildet wird.
- Wertvolle Edelsteine
Edelsteine sind kristalline Strukturen im Grunde genommen dieselbe Verbindung, jedoch mit kleinen Teilen von Verunreinigungen, die häufig für die Farbe von ihnen verantwortlich sind.
Diamant
Es besteht nur aus Kohlenstoff und enthält keine Verunreinigungen, weshalb es keine Farbe hat. Der Diamant hat Kubikkristalline Struktur (isometrisch-hexoktaedrisch) und ist das am härtesten bekannte Material.
Quarz
Es besteht aus Kieseloxid, es ist normalerweise farblos oder weiß. Seine kristalline Struktur ist trigonal-Trapezoédrica.
Rubin
Es besteht aus Aluminiumoxid mit Chromverunreinigungen, die ihm seine charakteristische rote Farbe verleihen. Bildet einen Hexagonales kristallines Netzwerk.
Saphir
Es ist auch ein Aluminiumoxidkristall, aber mit Unreinheiten von Titan und Eisen, die für ihre blaue Farbe in verschiedenen Farbtönen verantwortlich sind. Wie der Rubin hat sechseckige Struktur.
Jade
Edelstein im Allgemeinen grün, hat Monokline Struktur Und es besteht aus Eisen-Magnesium-Calcio-Silikat.
Topas
Es ist farblos mit einem Ortorrombische Struktur von Aluminiumhydroxid-Silicat-Fluorid.
Gelöste Übungen
Übung 1
Ermitteln Sie die Beziehung zwischen dem Netzwerkparameter und dem Atomradius für ein Kubiknetzwerk F.
Es kann Ihnen dienen: Theorie des Urknalls: Merkmale, Stufen, Beweise, Probleme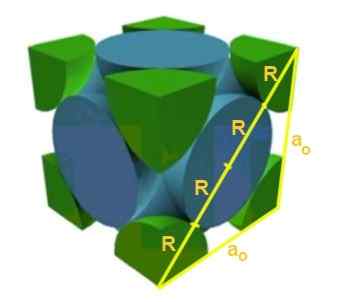
Lösung: In erster Linie wird angenommen, dass Atome als Kugeln in "Kontakt" miteinander als Kugeln dargestellt werden, wie in der Abbildung gezeigt. Es wird ein Rechteck -Dreieck gebildet, in dem es erfüllt ist:
(4 r)^2 = a^2 + a^2 = 2 a^2
Sie haben also, dass die Edge-Radio-Beziehung lautet:
A/r = 4/√2
Übung 2
Finden Sie die Beziehung zwischen dem Netzwerkparameter und dem Atomradius für ein Kubiknetzwerk I (Körper zentriert).
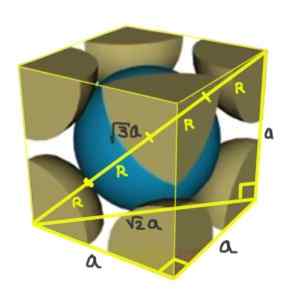
Lösung: Atome sollen als alle Radius -R -Kugeln in "Kontakt" miteinander dargestellt werden, wie in der Abbildung gezeigt.
Zwei Rechtecke werden zu einer von Hypotenusa √2a und der anderen von Hypotenuse √3a gebildet, wie durch die Verwendung des pythagoräischen Theorems demonstriert werden kann. Von dort aus müssen Sie eine Beziehung zwischen dem Netzwerkparameter und dem Atomradius für ein kubisches Netzwerk I (zentriert im Körper) lautet:
A/r = 4/√3
Übung 3
Finden Sie den Packfaktor F für eine Einheitszelle einer Kubikstruktur F (Kubikmitte auf Gesichtern), in der Atome Funk R und "Kontakt" haben.
Lösung: Der Packfaktor F ist definiert als das Verhältnis zwischen dem von den Atomen in der Einheitszelle besetzten Volumen und dem Volumen der Zelle:
F = vAtome / VZelle
Wie oben gezeigt, beträgt die Anzahl der Atome pro Zelle der Einheit eines Kubiknetzes, das sich auf Gesichter befindet, 4, daher ist der Packfaktor:
F = 4 [4πr^3 /3] /[a^3] =…
… 4 [4πr^3/3]/[4r/√2]^3 = (√2) π/6 = 0,74
Verweise
- Kristallstrukturen Akademisches Ressourcenzentrum. [PDF]. Abgerufen am 24. Mai 2018 von: Web: Web.ich s.Edu
- Kristalle. Abgerufen am 26. Mai 2018 von: theledco.com
- Pressebücher. 10.6 Latice -Strukturen in kristallinen Feststoffen. Abgerufen am 26. Mai 2018 von: OpenTextBC.AC
- Ming. (30. Juni 2015). Typen Kristallstrukturen. Abgerufen am 26. Mai 2018 von: Crystalvisions-Film.com
- Helmestine, Anne Marie, ph.D. (31. Januar 2018). Arten von
- Kittel Charles (2013) Solid State Physics, Physik der Kondensat Materie (8. Ausgabe). Wiley.
- Khi. (2007). Kristalline Strukturen. Abgerufen am 26. Mai 2018 von: Folk.Ntnu.NEIN
- Wikipedia. Bravais Latices. Abgerufen von: in.Wikipedia.com.
- « Konvexe Polygondefinition, Elemente, Eigenschaften, Beispiele
- Lichtergieeigenschaften, Typen, erhalten, Beispiele »

