Hebelregel
- 3514
- 367
- Lewis Holzner
Was ist die Hebelregel??
Der Hebelregel Es handelt sich um ein mathematisches Verfahren, das es ermöglicht. Es ist nicht nur mathematisch, sondern auch ziemlich grafisch und durchsetzungsfähig und ist bei physikalisch -chemischen und technischen Berechnungen sehr nützlich.
Diese Regel gilt für Phasendiagramme für binäre Systeme, unabhängig von der Art des Systems selbst. Das heißt, die Phasen können wie bei den Legierungen solide sein; oder flüssig und gasförmig, wie wir in Systemen im Gleichgewicht des Flüssigkeitsdampfes sehen.
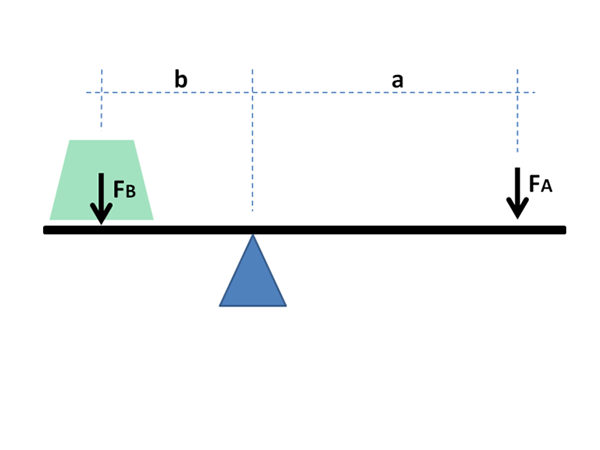
 Das physikalische und mathematische Prinzip des Hebels wird auch für chemische Zwecke und in der Physik der Materialien verwendet. Quelle: Jimbowley, CC BY-SA 3.0, über Wikimedia Commons
Das physikalische und mathematische Prinzip des Hebels wird auch für chemische Zwecke und in der Physik der Materialien verwendet. Quelle: Jimbowley, CC BY-SA 3.0, über Wikimedia Commons Die Hebelregel kann direkt unter Berücksichtigung der Wertegrafik in der Achse der Abszisse angewendet werden, wobei die globalen Fraktionen oder Prozentsätze der flüchtigsten Komponente normalerweise im Fall von Flüssigkeiten verlaufen. oder feuerfest, im Fall von Metallen in ihren Legierungen.
Wie nachstehend zu sehen ist, ist sein Name auf die immense Ähnlichkeit mit den mathematischen Ausdrücken zurückzuführen.
Die Hebelarme müssen ausgleichen, um die Massen der Lasten auszugleichen. Bei Phasendiagrammen, Brüchen und Mol der Phasen im Materialgleichgewicht.
Erläuterung
Grafische Aspekte
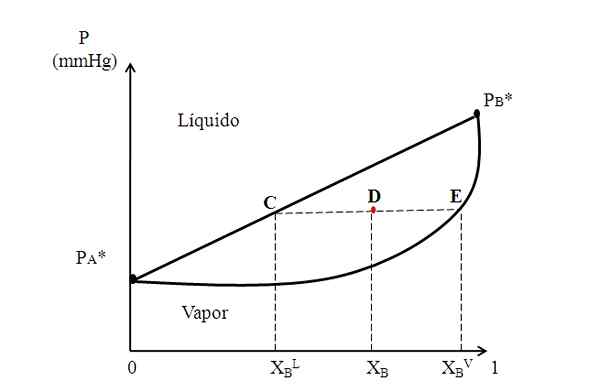 Hypothetisches binäres Diagramm, bei dem eine Bindungslinie die Zusammensetzungen der Flüssigkeits- und Dampfphasen zeigt. Quelle: Gabriel Bolívar.
Hypothetisches binäres Diagramm, bei dem eine Bindungslinie die Zusammensetzungen der Flüssigkeits- und Dampfphasen zeigt. Quelle: Gabriel Bolívar. In der Mitte des oben genannten Diagramms haben wir einen Bereich, in dem Flüssigkeit und Dampf koexistieren; Das heißt. Über diesem Bereich ist die Mischung von A und B flüssig und darunter ist Soda aufgrund des geringeren Drückens.
Betrachten Sie nun eine Mischung mit einer X -KompositionB und deren Druck es an Punkt D positioniert. Wir zeichnen aus dem Punkt D einer horizontalen Linie, die die Linie und die Kurve an den Seiten berührt und die Punkte C bzw. E entspricht. Diese Linie, die die Punkte C, D und E, C-D-E vermittelt, ist diejenige, die als Gewerkschaftslinie bekannt ist und sie in Richtung der Achse projiziert und uns den Druck des Systems geben muss.
Es kann Ihnen dienen: Wasseralkalität: Was ist, Entschlossenheit und WichtigkeitAnschließend zeichnen wir aus diesen Punkten andere Linien senkrecht zur Bindungslinie, die die x -Achse spielen. Da Punkt E auf der Dampfkurve ruht, haben wir die molare Fraktion von B in der Dampfphase (xBV). Ebenso gibt uns Punkt C auf der geraden Flüssigkeitslinie den molaren Anteil von B in der Flüssigkeitsphase (xBL).
Die Hebelregel basiert genau auf der Bindungslinie und den Entfernungen zwischen xBL, XB und xBV.
Mathematischer Abzug
Der globale molare Anteil von B entspricht:
XB = NB / (NL + NV)
Wo NB Sie sind die gesamten Mol von B sowohl in der Flüssigkeits- als auch in der Dampfphase und der Dampfphase und sind NL Und NV sind die jeweiligen Maulwürfe für diese Phasen. Clearing NB wir werden haben:
NB = XBNL + XBNV (1)
Andererseits, NB Es ist auch gleich:
NB = NBL + NBV
= XBLNL + XBVNV (2)
Jetzt geben uns die Gleichungen (1) und (2) aus:
XBNL + XBNV = XBLNL + XBVNV
Und neu ordnen:
NL(XB - XBL) = NV(XBV - XB) (3)
NL(C-d) = NV(VON)
Diese letzten beiden mathematischen Ausdrücke sind die Hebelregel. Beachten Sie, dass xB - XBL Es ist der Abstand zwischen den Punkten C und D; und xBV - XB, Es ist der Abstand zwischen den Punkten D-E: den beiden Hälften der Bindungslinie (Hebelarme).
Diese Gleichung ist dem der Beschreibung des Gleichgewichts der Massen auf einem Rocker mit Fullcro sehr ähnlich:
M1l1 = m2l2
Daher ermöglicht die Hebelregel uns, die gesamten Maulwürfe zu berechnen NL Und NV vorausgesetzt, dass die gesamten Mol der Mischung bekannt sind, NT (NT = NL + NV).
Zweite Form
Der vorherige Ausdruck für die Hebelregel dient dazu, die Größen (Massen, Maulwürfe usw. zu berechnen.) der Phasen im Gleichgewicht. Die bekannteste Version der Hebelregel ermöglicht es uns jedoch, die Brüche oder Prozentsätze jeder Phase zu berechnen, wobei wir nur die Entfernungen zwischen x einnehmen könnenB, XBL und xBV.
Betrachten Sie dasselbe System oben mit einer anderen Form der Hebelregel:
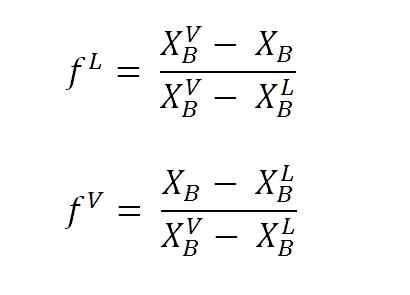 Gleichungen zur Berechnung von Flüssigkeits- und Dampffraktionen unter Verwendung der Hebelarme. Quelle: Gabriel Bolívar.
Gleichungen zur Berechnung von Flüssigkeits- und Dampffraktionen unter Verwendung der Hebelarme. Quelle: Gabriel Bolívar. Wo F L Und F VEs handelt. Beachten Sie das natürlich, F L Und F V Sie haben keine Einheiten; während NL Und NV Ja, sie haben Einheiten (Maulwürfe, Gramm usw.).
Kann Ihnen dienen: ReaktionswärmeBeispiele
Methode 1
In einem Behälter sind 28 Mol B und 12 Mol A gemischt. Bestimmen Sie die Mengen und Molfaktionen für die gebildeten Phasen.
Wir berechnen xB:
XB = (28 Mol B)/ (28 Mol B + 12 Mol A)
= 0.7
Dieser Wert entspricht xB des oberen Diagramms. Die Interceptions geben uns ungefähr die folgenden Werte für xBL und xBV:
XBL = 0.41
XBV = 0.94
Mit der Hebelregel:
NL(XB - XBL) = NV(XBV - XB)
Und das zu wissen NT = NL + NV, Und? NT = 40 Maulwürfe, dann klären wir klar NL entweder NV Abhängig von der anderen:
NL(XB - XBL) = (40 Maulwürfe - NL) (XBV - XB)
Neu anordnen und löschen NL wir werden haben:
NL = (40 Mol) (xBV - XB) / (XBV - XBL)
Erinnert sich dieser Ausdruck nicht an den von? F L? Jetzt ersetzen wir:
NL = (40 Mol) (0.94 - 0.70) / (0.94 - 0.41)
= 18.11 Maulwürfe in flüssiger Phase
Wir können berechnen NV In zwei Wegen:
NV = NL(XB - XBL) / (XBV - XB)
entweder
NV = 40 Maulwürfe - 18.11 Maulwürfe
= 21.89 Maulwürfe in Dampfphase
Methode 2
Was ist, wenn wir zuerst berechnen F L Und F V?
F L = (XBV - XB) / (XBV - XBL)
= (0.94 - 0.70) / (0.94 - 0.41)
= 0.4528 oder 45.28%
Das heißt 45.2% der Maulwürfe befinden sich in einer flüssigen Phase, da diese Menge gleich ist:
NL = F LNT
= (0.4528) (40 Maulwürfe)
= 18.11 Maulwürfe
UND F V Wir können es auf zwei Arten gleichermaßen berechnen:
F V = 1 - F L
entweder
F V = (XB - XBL) / (XBV - XBL)
Sein Wert sein:
F V = 0.5472 oder 54.72%
Und deshalb, NV Es wird gleich sein:
NV = F VNT
= (0.5472) (40 Mol)
= 21.89 Maulwürfe
Beachten Sie, dass die Anwendung der beiden Formen der Hebelregel als alternative Berechnungsmethoden die gleichen Ergebnisse erzielt werden können. Methode 2 scheint direkter und einfacher; Aber wenn es sorgfältig beobachtet wird, sobald die Lichtung aufgelöst wird NL entweder NV, Es ist zu sehen, dass beide Methoden tatsächlich ebenso einfach sind.
Gelöste Übungen
Als nächstes werden zwei weitere Übungen aufgelöst, bei denen jetzt die betrachteten Systeme einen flüssig-soliden und nicht flüssigen Vapor umfassen. Außerdem sind die Diagramme in Bezug auf die Systemtemperatur und nicht in ihrem Druck grafisch.
Übung 1
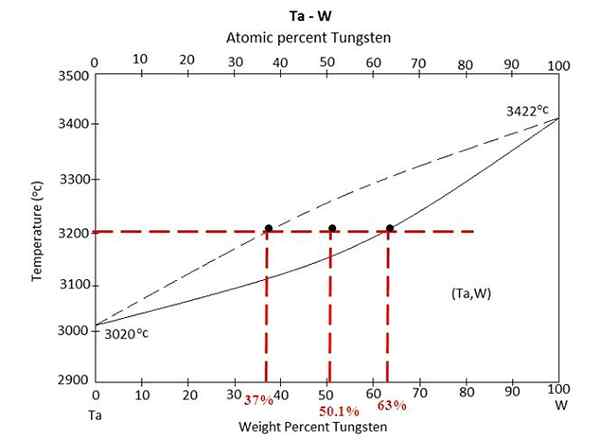 Phasendiagramm für eine Legierung zwischen Tantalo und Wolfram. Quelle: Materialpedia, CC BY-SA 4.0, über Wikimedia Commons
Phasendiagramm für eine Legierung zwischen Tantalo und Wolfram. Quelle: Materialpedia, CC BY-SA 4.0, über Wikimedia Commons Wir haben das Phasendiagramm über einer Legierung zwischen Tantalo und Wolfram, Ta-W. Auf der X -Achse sind die weltweiten Massenprozentsätze von Win.
Innerhalb des flüssigen Gleichgewichtsbereichs (Ta+W) und fester (Legierung) befindet sich eine Mischung bei 3200 ° C. Bestimmen Sie die Massen jeder Phase unter der Annahme, dass 100 Gramm der Legierung erhitzt wurden.
Es kann Ihnen dienen: Metalle, Nicht -Metals und MetalloidenVerfahren
Diesmal wird die Übung unter Verwendung der zweiten Form der Hebelregel gelöst. Die Gewerkschaftslinie sagt uns: In der festen Phase haben wir 63% Wolfram, während wir in der flüssigen Phase 37% Wolfram haben. Dies liegt daran, dass der Wolfram auf eine höhere Temperatur (3422 ºC) als die Tantal (3020 ° C) schmilzt (3020 ºC).
Also haben wir:
W%S oder wS= 63%
W%L oder wL= 37%
Und auch:
W0 = 50.1%
Wir wenden die Hebelregel auf F L:
F L = (63% - 50.1%) / (63% - 37%)
= 0.4961 oder 49.61%
Beachten Sie, dass der Abstand, der der flüssigen Phase entspricht.
Die Masse der flüssigen Phase ist daher:
(0.4961) (100 Gramm) = 49.61 geschmolzene Gramm
Und die feste Phase entspricht:
100 Gramm - 49.61 Gramm = 50.39 Gramm Legierung reich an Wolfram
Übung 2
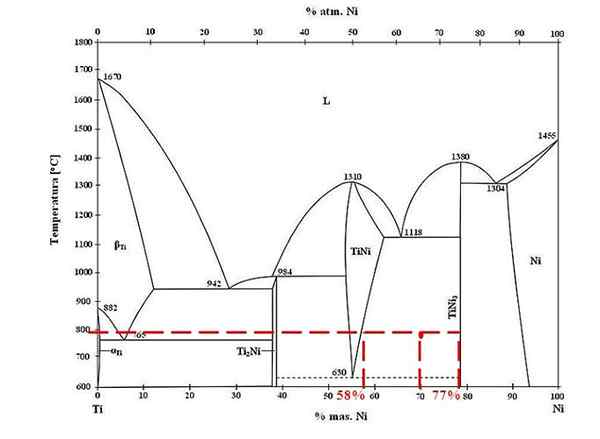 Phasendiagramm für Titan-Nickel-Legierungen. Quelle: Doomgiver, CC BY-SA 3.0, über Wikimedia Commons
Phasendiagramm für Titan-Nickel-Legierungen. Quelle: Doomgiver, CC BY-SA 3.0, über Wikimedia Commons Für die Titan- und Nickellegierung bei 800 ° C und mit 70% Nickel bestimmen Sie, wie viel von Tini und Tini3 Sie sind anwesend.
Verfahren
Diesmal fragen sie nur nach den Massenbrüchen jeder Phase. Der rote Punkt befindet sich im Gleichgewichtsbereich zwischen den Tini- und Tini -Phasen3, Wessen Kurven ist dort, wo es die Gewerkschaftslinie spielt, die zu den Werten von 58% oder für die Tini -Phase und 77% oder für die Tini -Phase fließt3.
Beachten Sie, dass der rote Punkt näher an der Tini -Phase liegt3 das der Tini -Phase. Dies bedeutet, dass es mehr Tini geben muss3 das Tini; Und damit der Abstand oder der Hebelarm, der Tini entspricht3 Es muss das längste sein, das Gegenteil (70%-58%).
Wenn wir dies wissen, werden wir berechnet, um dies zu berechnen F Tini3:
F Tini3 = (70% - 58%) / (77% - 58%)
= 0.6316 oder 63.16%
In der Tat 63.16% der Legierung entsprechen der Tini -Phase3. In der Zwischenzeit entspricht die Tini -Phase:
1 = F Tini3 + F Tini
F Tini = 1 - F Tini3
= 0.3684 oder 36.84%
Zusammenfassend können wir sagen.
Verweise
- Walter J. Moore. (1963). Physikalische Chemie. In der chemischen Kinetik. Vierte Ausgabe, Longmans.
- Iran. Levine. (2009). Prinzipien der Physikochemie. Sechste Ausgabe. Mc Graw Hill.
- Wikipedia. (2020). Hebelregel. Abgerufen von: in.Wikipedia.Org
- Michael Adewumi. (18. Mai 2020). Die Hebelregel. Erholt von: Eng.Librettexts.Org
- Adam Warren. (1997). Phasendiagramme: Bindungslinien und die Hebelregel. Erholt von: Southampton.AC.Vereinigtes Königreich
- Universität von Cambridge. (2020). Die Hebelregel. Abgerufen von: doitpoms.AC.Vereinigtes Königreich

