Markovnikov Regel
- 3376
- 562
- Ibrahim Steuk
Was ist Markovnikovs Regel?
Der Markovnikov Regel Es ist eine empirische Regel, die 1869 vom russischen Chemiker Vladimir Markovnikov formuliert wurde und zur Vorhersage der Regioselektivität der Produkte einer elektrophilen Ergänzung verwendet wird. Noch heute ist es immer noch in Kraft und zeigt seine Einfachheit in der Art und Weise, wie der Mechanismus mehrerer organischer Reaktionen kommt.
Diese Regel gilt insbesondere für Alkene in ihren Hydrohalogenierungsreaktionen. Daher ermöglicht es vorherzusagen, was die Mehrheitsprodukte sein werden, wenn Alkene und Alkines mit HX reagieren (HF, HCL, HBR und HI).
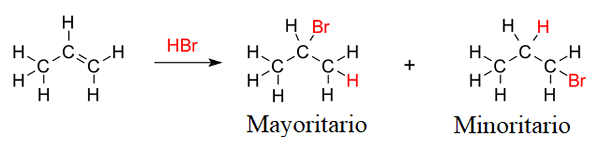 Wertschätzung der Markovnikov -Regel bei der Hydrohalogenierung des Propeno. Quelle: V8RIK, CC BY-SA 3.0, über Wikimedia Commons
Wertschätzung der Markovnikov -Regel bei der Hydrohalogenierung des Propeno. Quelle: V8RIK, CC BY-SA 3.0, über Wikimedia Commons Nehmen wir zum Beispiel die Hydrobromierung des Propeno oder Propylens (überlegenes Bild) an,. Die Regel von Markovnikov sagt voraus, dass das Mehrheitsprodukt das ist, in dem das Bromatom mit dem Kohlenstoff des Zentrums verbunden ist. Während des Moll -Produkts endet das Brom zu dem Doppelbindungskohlenstoff.
Beachten Sie, dass das Mehrheitsprodukt das Wasserstoffatom mit terminalem Kohlenstoff in Verbindung bringt. Dieser letzte Punkt ist am einfachsten zu merken: Der HX-Wasserstoff geht zum Kohlenstoff der Doppelbindung mit mehr Wasserstoff- oder C-H.
Prinzipien der Markovnikov Regel
Elektrophile Addition
Zu den doppelten Bindungen von Alkenen oder Alkinen. Der HX hat ein schlechtes Elektronenatom, das H ist, und ein Atom, das reich an Elektronen ist, nämlich x.
Daher kann HX als h dargestellt werdenδ+-Xδ-, Die Region h sein hδ+ Anfällig für Elektronen in diesem Fall doppelte Bindung eines Alkens, der den elektrophylischen Angriff stattfindet (siehe Bild unten).
Kann Ihnen dienen: Phenylessigsäure: Struktur, Eigenschaften, Verwendungen, EffekteCarbokationsstabilität
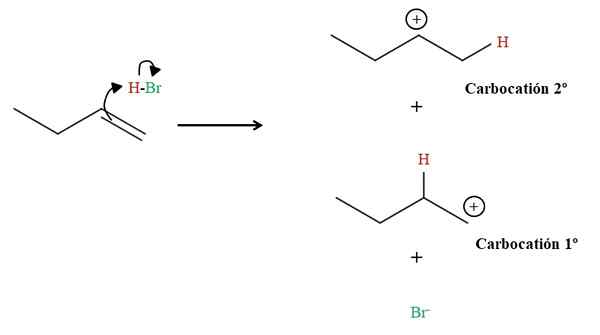
 Bildung der beiden Karbokationen in der Hidrobromierung von 1-Butene. Quelle: Gabriel Bolívar über Molview.
Bildung der beiden Karbokationen in der Hidrobromierung von 1-Butene. Quelle: Gabriel Bolívar über Molview. Wie oben zu sehen ist, greift das 1-Buten-Doppelbindungsbindung den HBO-Wasserstoff an. Dabei "öffnen" die Elektronen der H-Br-Bindung in Richtung des Bromatoms und bilden eine Carbokation und das Anion BR-. Es besteht jedoch die Möglichkeit, zwei Karobokationen zu bilden: eine primäre (1.) und die andere Sekundär (2.).
Jede Carbokation ist eine Zwischenverbindung, von der das Endprodukt abgeleitet wird. Wenn es zwei Karbationen gibt, haben wir zwei Produkte: 2-Bromobutano und 1-Bromobutano. Die Br- Es wirkt als Nucleophil, der eine der beiden Karbokalationen angreift:
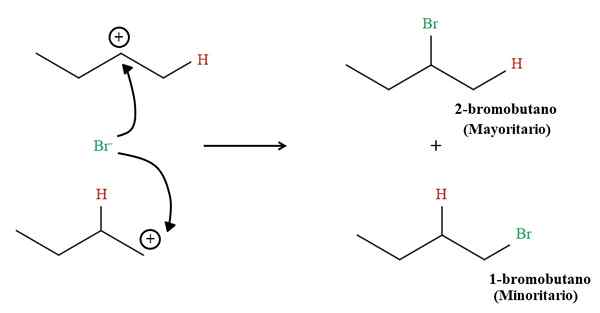 1-Buten-Hydrobromierungsprodukte. Quelle: Gabriel Bolívar über Molview.
1-Buten-Hydrobromierungsprodukte. Quelle: Gabriel Bolívar über Molview. Der Anteil beider Produkte beträgt jedoch nicht 50%; Der 2-Bromobutano tritt viel größer auf als der 1-Bromobutan.
Der Grund dafür ist, dass die 2. Carbokation stabiler ist als die 1. Carbokation, da seine positive Belastung durch benachbarte Kohlenstoffatome besser stabilisiert ist. Während in Carbocation 1 trägt das Wasserstoffatom nicht fast eine elektronische Dichte in diese positive Belastung (für Induktion oder Hyperkonjugation).
Die Reichen werden reicher
Markovnikovs Regel wurde aus den endgültigen Beobachtungen geboren, und von ihnen konnten die oben dargestellten Mechanismen in Betracht gezogen werden, um sie zu erklären.
Ohne die Notwendigkeit, diese Mechanismen immer zu erfassen oder die Stabilität von Vermittlungskarbokationen abzuziehen, wird die einfache Regel verwendet: Bei einer elektrophilen Addition werden Wasserstoffatome mit dem Doppel -Kohlenstoff mit mehr Wasserstoffatomen gerichtet. Somit wird der am stärksten hydrierte Kohlenstoff noch hydrierter.
Kann Ihnen dienen: Was sind Wasseranomalien??Andererseits endet das Atom X in diesem Fall das BR im Kohlenstoff der Doppelbindung mit mehr C-C-Bindungen oder wird mehr durch andere Atome ersetzt, die kein Wasserstoff sind. Denn im 1-Buten ist sein terminaler Kohlenstoff = cho2, Dies ist derjenige, der Wasserstoff erhält, um sich in die -ch -Gruppe zu verwandeln3.
Beispiele
Der Fall der in der Hydrobromierungsreaktion angewendeten Markovnikov -Regel wurde oben beobachtet. Es gilt auch für Hydroclination, Hydroiodation, Hydroamination und Hydratationsreaktionen, entweder für Alkene oder Alkine.
Im folgenden Abschnitt werden einige zusätzliche Beispiele als Übungen angesehen.
Gelöste Übungen
Übung 1
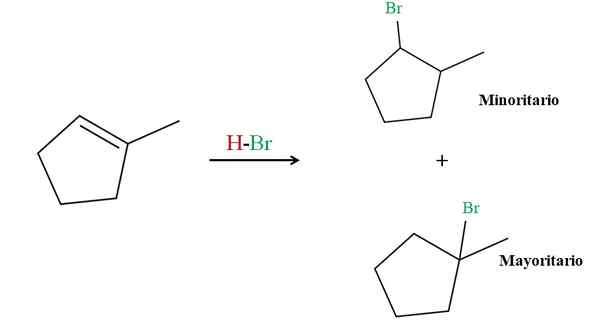 Hydromation des 2-Methylciclopentins. Quelle: Gabriel Bolívar über Molview.
Hydromation des 2-Methylciclopentins. Quelle: Gabriel Bolívar über Molview. Markovnikovs Regel sagt, dass die HBR H für die obere Reaktion mit mehr Wasserstoffatomen zum Doppelbindungskohlenstoff gehen muss. In diesem Fall entspricht es dem obigen Kohlenstoff, da der Kohlenstoff rechts mit Cho verbunden ist3, Es hat nicht einmal Wasserstoffatome.
Somit geht der HBR -Wasserstoff in den Kohlenstoff oben, während das BR endet mit Kohlenstoff rechts (Mehrheitsprodukt). Andererseits ist der Br, wenn Wasserstoff auf der rechten Seite mit dem Kohlenstoff verbunden ist, der BR auf den darüber liegenden Kohlenstoff (kleineres Produkt) gerichtet ist (kleineres Produkt).
Beachten Sie, dass das Mehrheitsprodukt aus einem dritten Halogenid besteht, der per Definition stabiler und stabilisiertere Auswirkungen von teilweise positiven Lasten ist. Während das Minderheitsprodukt ein 2., weniger stabiler Halogenid ist.
Beide Produkte, die Mehrheit und die Kleinern. Diese Art von Minderheitsprodukt gegen die Markovnikov -Regel ist als Antimarkovnikov -Produkt bekannt.
Kann Ihnen dienen: Referenzelektrode: Eigenschaften, Funktion, BeispieleÜbung 2
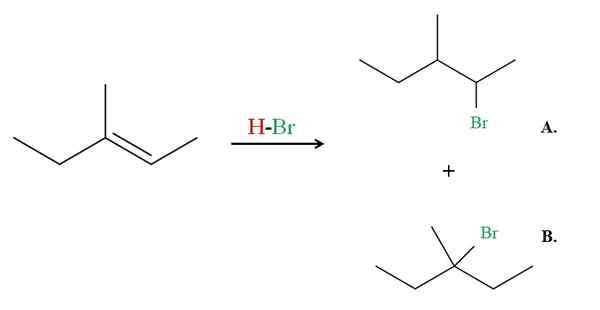 Hydrobromierung von 3-Methyl-2-Penten. Quelle: Gabriel Bolívar über Molview.
Hydrobromierung von 3-Methyl-2-Penten. Quelle: Gabriel Bolívar über Molview. Sehen Sie nun das Beispiel von 3-Methyl-2-Pentene.
Wenn dies beobachtet wird, hat der rechte Kohlenstoff der Doppelbindung ein h, während der links eine h. Daher wird der H des HBR zu diesem Kohlenstoff gehen, der Kohlenstoff muss in das Zentrum gehen, um Produkt B zu verursachen. Produkt B ist die Mehrheit, weil es wieder ein 3. Halogenid ist, wobei das Produkt ein Haluro 2. ist.
Übung 3
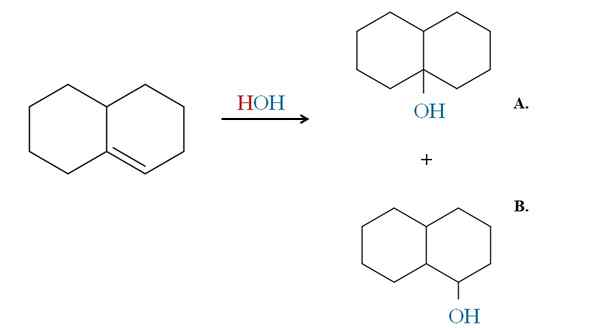 Beispiel für die Markovnikov -Regel bei der Flüssigkeitszufuhr eines zyklischen Alkens. Quelle: Gabriel Bolívar über Molview.
Beispiel für die Markovnikov -Regel bei der Flüssigkeitszufuhr eines zyklischen Alkens. Quelle: Gabriel Bolívar über Molview. Die vorherigen Beispiele hätten dieselben Produkte generiert, wenn anstelle von HBR HCL und HI verwendet würden. Das gleiche ist das gleiche wie bei H2O in einer Hydratationsreaktion, die durch Säure und Wärme katalysiert wurde. Oh kommt, um das HX -Atom zu ersetzen.
Daher sagt uns Markovnikovs Regel, dass OH in der oben elektrophilen Ergänzung zum Kohlenstoff der am meisten ersetztesten Doppelbindung mit weniger Wasserstoff geht.
So ist Produkt A die Mehrheit und Produkt B die Minderheit. Beachten Sie noch einmal, dass das Produkt A ein 3. Alkohol und Produkt B A 2. Alkohol ist.
Verweise
- Morrison, r. T. und Boyd, r, n. (1987). Organische Chemie. 5. Ausgabe. Editorial Addison-Wesley Interamerikaner.
- Carey f. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Braten. (2011). Organische Chemie. (10. Ausgabe.). Wiley Plus.
- Wikipedia. (2020). Markovnikovs Regel. Abgerufen von: in.Wikipedia.Org
- Steven a. Hardinger. (2017). Illustriertes Glossar der organischen Chemie: Markovnikovs Regel. Erholt von: Chem.UCLA.Edu
- Gamini Gunawardena. (24. August 2020). Markovnikovs Regel. Chemistry Librettexts. Erholt von: Chem.Librettexts.Org
- Die Herausgeber von Enyclopaedia Britannica. (17. September 2013). Markovnikovs Regel. Erholt von: Britannica.com
- DR. S. Gevorg. (2020). Organische Chemie: Markovnikovs Regel mit Praxisproblemen. Erholt von: Chemistroysteps.com

