Safranineigenschaften, Verwendung, Techniken, Toxizität
- 1831
- 420
- René Riediger
Der Safranin Es handelt.
Es wird auch Safranin oder Basic Red Dimethyl in seiner zusammenfassenden Form bezeichnet, da sein wissenschaftlicher Name 3,7-Diamino-2,8-Dimethyl-5-Phenylphenylphenyll beträgtzwanzigH19N4 Cl.
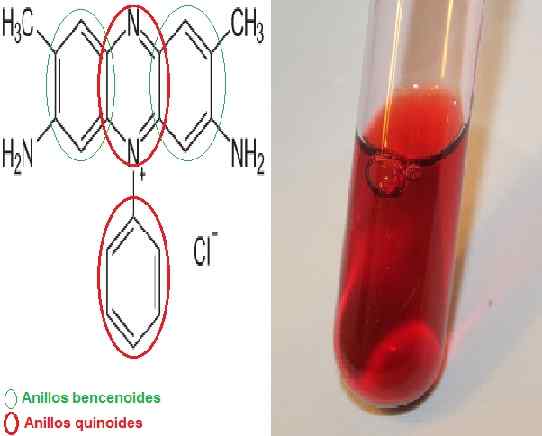
 Chemische Struktur von Safranin, die die Benzol- und Chinoidringe/ die wässrige Lösung von Safranin angibt. Quelle: Neurotoger [Public Domain] Herausgegeben von MSC. Marielsa Gil/Lhchem [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]
Chemische Struktur von Safranin, die die Benzol- und Chinoidringe/ die wässrige Lösung von Safranin angibt. Quelle: Neurotoger [Public Domain] Herausgegeben von MSC. Marielsa Gil/Lhchem [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]] Es gibt eine Variante namens Trimethyle-Safranin, aber es gibt keinen signifikanten Unterschied zwischen beiden Substanzen.
Safranin ist ein monochromatischer Farbstoff und nach den Eigenschaften der chemischen Formel eine positive Ladungssubstanz. Daher hat es eine Affinität zu negativ belasteten Strukturen. Diese Strukturen werden rot gefärbt.
Diese Eigenschaft gibt Anwendbarkeit in vielen histologischen Techniken, um verschiedene zelluläre Strukturen sowohl aus eukaryotischer als auch aus prokaryotischer Organismen zu färben.
Safranin wird als Kontrastfarbstoff in wichtigen und bekannten Routine -Anwendungstechniken in der Bakteriologie verwendet. Diese Techniken sind: Gram-Hucker-Färbung, Schaeffer-Fulton-Färbung für Sporen oder Bakterienkapseln unter anderem.
[TOC]
Eigenschaften
Die Farbe des Safrans (Gewürz aus den Stigmen der Blume von erhalten Krokus sativ) war die Inspiration, den Namen dieses Farbstoffs zu geben. Aus dem Begriff kommt Safran der Name Safranin. Das liegt an der großen Ähnlichkeit zwischen der Farbe von Safran und der Färbung, die dieser Farbstoff bietet.
Safranin wird als Kristalle oder Pulver erreicht, wobei beide Präsentationen in Wasser löslich sind. Safraninfarbstoff hat keinen Geruch. Rote Strukturen färben. Strukturen, die den Safraninfarbstoff anziehen, werden als Safranophile bezeichnet.
Strukturell ist das Safranin komplex, hat zwei Benzolring bis zu den Enden und befinden sich in der Mitte die beiden Chinoidringe, wo sich Kation N befindet+. Das Zentrum der Struktur ist das System, das für die Bereitstellung von Farbe verantwortlich ist. Durch dieses Merkmal wird dieser Farbstoff in Kategorie II klassifiziert.
Verwenden
Safranin wird verwendet, um verschiedene Strukturen zu färben. Insbesondere hebt Kulchitskys Zellen im Magen -Darm -Trakt vor, auch als Enterocromofine -Zellen bezeichnet.
Es ist in der Lage, Mikroorganismen der Familie zu färben Rickettsiaaceae. Ebenso wird es in verschiedenen Techniken verwendet, wie z Brucella.
Andererseits wird das Safranin in der Färbungstechnik von Schaeffer Fulton Sporen und in der Färbung von Gram-Hucker verwendet. In beiden Techniken arbeitet Safranin als Kontrastfarbstoff.
Kann dir dienen: indischIm ersten haben die Sporen die Farbe des Grünen von Malachit und der Rest der Strukturen werden vom Safranin rot. Im zweiten Verlust von Gramm negativ.
Zusätzlich wird Safranin in der Bakteriologie verwendet, um Brucella -Agar mit einer 1: 5000 -Safraninverdünnung herzustellen. Dieses Medium dient dazu, die Art zu unterscheiden Brucella Suis der übrigen Spezies. Brucella melitensis Und Brucella abortus wachsen in diesem Medium aber B. Suis Es wird gehemmt.
Im agroindustriellen Bereich wurde das Safranin bei 2,25% verwendet und 1:10 verdünnt, um Stammproben aus der Zuckerrohrpflanze zu färben.
Diese Pflanze wird üblicherweise von Bakterien betroffen Leifsonia Xyli Subs. Xyli, Wer schädigt den Xilema der Pflanze. Die gefärbten Stängel werden bewertet, um die Funktion der Xylemgefäße zu bestimmen.
Techniken im Bereich der Bakteriologie
Castañeda -Flecken für R -FleckIckettsias
Ein Blut- oder Gewebeabstrich wird in eine Pufferlösung gelegt (Phosphatdämpfung pH 7,6). Es darf spontan trocknen und dann 3 Minuten lang mit Methylenblau bedeckt und mit Safranin zusammengezogen werden. Rickettsias farbig blau und im Gegensatz zum roten Hintergrund.
Modifizierte Koster -Färbung für Brucella
Ein Abstrich wird durchgeführt und Flammenwerbung im Leichter zur Fixierung. Anschließend ist es mit einer Mischung aus 2 Teilen gesättigter wässriger Safranin mit 3 Teilen KOH 1 mol/l Lösung für 1 Minute bedeckt. Eine Wäsche mit destilliertem Wasser wird durchgeführt und 1% Fenado Methylenblau.
Wenn die Probe geschlechtsspezifische Bakterien enthält Brucella Diese werden in einem blauen Hintergrund orange beobachtet.
Bakterienkapseln Färbung
Eine Mischung aus bakterieller Suspension mit chinesischer Tinte wird durchgeführt und Safranin wird zugegeben. Ein rötlicher Halo wird am Mikroskop um jede Bakterienkapsel mit einem schwarzen Hintergrund beobachtet.
Kann Ihnen dienen: reine SubstanzenFärbung von Sporen Schaeffer Fulton
Eine erweiterte mit der Bakteriensuspension wird durchgeführt. Dann ist es befestigt, zu heizen. Es ist mit 5%Malachitgrün bedeckt, häufig flammen Sie bis zur Emission von Dämpfen. Der Vorgang wird 6-10 Minuten wiederholt. Schließlich wird es mit Wasser gewaschen und 30 Sekunden lang mit 0,5% Safranin eingestellt. Die Bacilli sind rot gefärbt und die grünen Sporen.
Gram-Hucker-Färbung
Eine erweiterte mit bakterielle Suspension wird durchgeführt und an Wärme befestigt. Die Lamina mit violettem Glas bis 1 Minute ist bedeckt. Dann wird Lugol als unter 1 Minute als unterbrochene Lösung platziert. Anschließend wird es mit Acetonalkohol verfärbt und schließlich 30 Sekunden lang mit Safranin eingestellt.
Gram -positive Bakterien sind blau violett und gram negative Bakterien von Rot.
Einige Labors haben die Gram-Hucker-Technik eingestellt, um die modifizierte Gram-Kopeloff-Technik einzusetzen. In letzterem wird Safranin durch Basisfuchsin ersetzt. Dies liegt daran Legionellen, Campylobacter Und Brucella.
Techniken im Histologiebereich
Kulchitsky -Zellfärbung (Enterokromofine)
Die Gewebeschnitte des Magen -Darm -Trakts mit Silberchlorid sind gefärbt. Dann ist es mit Natriumthiosulfat verfärbt und schließlich mit Safranin eingestellt.
Kulchitsky -Zellen werden unterschieden, weil sie mit schwarzbraunen Granulaten präsentiert werden.
Färbung zur Arthrose -Erkennung
Safranin, weil es eine positive Belastung, Carboxy- und Sulfatgruppen von Glykosaminoglykanen hat, bindet sehr gut. Diese sind Teil der Proteoglykane, die Gelenkknorpel bilden. In diesem Sinne kann beim Färben mit Safranin oder in diesem Sinne ermittelt werden, ob ein Knorpelverlust vorliegt oder nicht.
Der Verlust von Knorpelgewebe kann über die Mankin -Skala gemessen oder auch als Osteoarthritis -Skala bezeichnet werden.
Die Technik wird dann erklärt: Der histologische Schnitt wird in ein Tablett mit Weigererts Eisenhämatoxylinlösung eingetaucht, dann wird er durch sauren Alkohol geleitet und mit Wasser gewaschen.
Setzen Sie den Färben fort. Um den Prozess zu beenden, wird es mit Alkoholen in unterschiedlichen Konzentrationen in aufsteigender Reihenfolge dehydriert. Der letzte Schritt erfordert, dass Xileno oder Xilol die Probe klären, um zu klären.
Kann Ihnen dienen: MetalloidenDie Blätter sind mit Kanada -Balsam konditioniert oder ähnlich wie bei einem Mikroskop beobachtet werden.
Mit dieser Technik sind die Kerne schwarz gefärbt, der grüne Knochen und der Knorpel, in dem die roten Proteoglykane gefunden werden.
Tincion zur Identifizierung von Makroalgas
Pérez et al. Im Jahr 2003 schlugen eine einfache und wirtschaftliche Technik vor, um die Makroalgas zu färben. Proben werden in histologischen Schnitten mit Paraffin hergestellt. Die Schnitte werden mit 1% Glycerin eingestellt, wodurch sich selbst vollständig trocken sein lässt. Dann wird es in Xylol platziert, um Paraffin zu beseitigen.
Der Schnitt wird rehydriert, so.
Anschließend wird es 5 Minuten lang mit einer 3: 1 -Mischung von 1% Safranin mit 1% Toluidinblau gefärbt, beide mit 50% Ethanol hergestellt. Die Mischung wird drei Tropfen Pikrinsäure zugesetzt, die als Untersuchung wirken.
Dann wird es durch die Alkoholschalen wieder dehydriert, aber diesmal aufsteigend. Schließlich wird es mit Xilol geklärt und die Stichprobe wird mit dem Kanada -Balsam zu beobachten, das zu beobachten ist.
Toxizität
Glücklicherweise ist Safranine ein Farbstoff, der keine Gefahr für diejenigen darstellt, die ihn manipulieren. Es ist ein harmloser Farbstoff, es ist nicht krebserregend und auch nicht brennbar.
In direktem Kontakt mit der Haut oder der Schleimhäute kann eine leichte Rötung des Gebiets ohne größere Komplikationen verursachen. Dazu wird empfohlen, den betroffenen Bereich mit viel Wasser zu waschen.
Verweise
- Garcia h. Safraninfarbstoff oder. Gesundheitstechnik, 2012; 1 (2): 83-85. Verfügbar bei: Medigraphic.com
- Gil m. Grammfärbung: Fundament, Materialien, Technik und Verwendung. 2019. Erhältlich bei: Lofede.com
- Gil m. Färbung von Sporen: Fundament, Techniken und Verwendung. 2019. Erhältlich bei: Lofede.com
- Safranin." Wikipedia, freie Enzyklopädie. 7. März 2017, 10:39 UTC. Vor 2019, 20:49 ist.Wikipedia.Org
- Pérez-Cortéz S., Vera B, Sánchez C. Nützliche Färbungstechnik in der anatomischen Interpretation von Graciliasis Tenuifrons Und Gracilaria chilensis (Rhodophyta). Bot Act. Venez. 2003; 26 (2): 237-244. Erhältlich bei: Scielo.Org.
- ALEIKA -Kirche, Peralta Esther Lilia, Alvarez Elba, Milián J, Matos Madyu. Verhältnis der Funktionalität der Xylemgefäße und des Vorhandenseins von Leifsonia xyli subp. Xyli. Rev. Gemüseschutz. 2007; 22 (1): 65-65. Erhältlich bei: Scielo.Sld

