Stoßdämpferlösungen

- 3757
- 1036
- Joy Hort
Wir erklären, was die Dämpfungslösungen, ihre Eigenschaften, Komponenten, Typen sind, und geben mehrere Beispiele an
 Die Schockabsorbungslösungen regulieren den pH -Wert um einen bestimmten Wert
Die Schockabsorbungslösungen regulieren den pH -Wert um einen bestimmten Wert Was sind Dämpfungslösungen?
Der Stoßdämpferlösungen, Auch Puffer, pH- oder Pufferregulatoren genannt, sind wässrige Lösungen, die durch schwache Säure und ihre konjugierte Base oder eine schwache Base und ihre konjugierte Säure gebildet werden.
Sie werden als Stoßdämpferlösungen bezeichnet, da sie die Fähigkeit haben, die Änderung des pH -Werts nach Zugabe von Säuren oder Basen in kleinen Mengen zu kissen, auch wenn es sich um starke Säuren oder Basen handelt.
Die Stoßdämpferlösungen sind sehr nützlich, da sie den pH -Wert konstant sein lassen. Es gibt viele chemische Reaktionen, die einen spezifischen und konstanten pH -Wert benötigen, um gut zu funktionieren.
Eigenschaften der morpainären Lösungen
Sie sind wässrige Lösungen
Sowohl das pH -Konzept als auch die pH -Skala sind in wässrigen Lösungen nur sinnvoll, sodass alle Puffer oder Dämpfungslösungen in Wasser hergestellt werden.
Sein Betrieb basiert auf dem Acid-Base-Gleichgewicht und den Prinzipien von Le Chatlier
Puffer basieren auf reversiblen Säure-/Basen -Dissoziationsreaktionen, die im Gleichgewicht liegen. Durch das Hinzufügen starker Säuren oder Basen zur Umwelt wird dieses Gleichgewicht gestört, sodass das System auf die Störung entgegenwirkt. So schaffen es Puffer, die großen Veränderungen im pH -Wert zu kissen.
Ihr pH-Wert kann leicht mit Henderson-Haselbalch-Gleichung berechnet werden
Unabhängig davon, welche Art von Stoßdämpferlösung, der pH-Wert vor und nach dem Zugabe kleiner Mengen starker Säuren oder Basen, kann er mittels der Henderson-hohaselbalch-Gleichung berechnet werden:
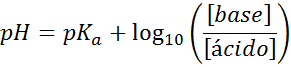
Wobei [Base] die molare Konzentration der Base (oder das Salz der konjugierten Base) und [Säure] auf die molare Konzentration der Säure (oder des Salzes der konjugierten Säure) bezieht.
Kann Ihnen dienen: elastische MaterialienSie können sowohl Säuren als auch Basen teilweise neutralisieren
Die Dämpfungslösungen bestehen aus einer Grundsubstanz und einer sauren Substanz, die Basen bzw. Säuren neutralisieren kann. Aus diesem Grund können sie den pH -Wert nach Zugabe sowohl starker Säuren als auch starken Basen kissen.
Der Betrieb hängt von der Temperatur ab
Der pH -Wert einer Pufferlösung hängt von der Säure oder Grundkonstante der Säure oder der schwachen Base ab, die sie enthält. Diese Konstante hängt von der Temperatur ab, daher hängt der Betrieb dieser Lösungen auch von der Temperatur ab.
Je konzentrierter, desto größer ist seine Fähigkeit, den pH zu kissen oder zu regulieren
Die Dämpfungskapazität hängt von der Gesamtkonzentration der Lösung ab. Je größer die Gesamtkonzentration der Pufferlösung ist, desto größer ist die Fähigkeit, Säuren oder starke Basen zu kolpieren.
Komponenten einer Dämpfungs- oder Pufferlösung
Chemisch werden Dämpfungslösungen nur durch zwei Komponenten gebildet. Diese Komponenten können eine schwache Säure sein, die mit einem Salz aus ihrer konjugierten Base oder einer schwachen Base gemischt wird, gemischt mit einem Salz seiner konjugierten Säure.
Es gibt zwei verschiedene Möglichkeiten, diese Komponenten in derselben Lösung zu erhalten, wie wir unten sehen werden:
1. Vorbereitung von Puffermischlösungen seiner Komponenten
Dies ist die direkteste Möglichkeit, eine Pufferlösung vorzubereiten. Dazu sind getrennte Lösungen von schwacher Säure (zum Beispiel Essigsäure) und ein konjugiertes Basensalz (zum Beispiel Natriumacetat) separate Lösungen hergestellt). Dann mischen beide Lösungen nach und nach bis zum gewünschten pH -Wert.
Es kann Ihnen dienen: Ion Ammonium (NH4+): Formel, Eigenschaften und Verwendung
- Lösungen werden nach und nach bis zum gewünschten pH gemischt
2. Herstellung von Puffern durch partielle Neutralisation einer Lösung einer schwachen Säure
In diesem Fall wird eine schwache Säurelösung mit der gewünschten Gesamtkonzentration hergestellt, und dann wird Natrium- oder Kaliumhydroxid nach und nach zugesetzt, bis er den gewünschten pH erreicht hat.
Arten von Pufferlösungen
Die Stoßdämpferlösungen können nach den Arten von Komponenten klassifiziert werden, die sie besitzen, oder nach ihrem endgültigen pH -Wert.
Gemäß den Arten von Komponenten:
- Schwacher und konjugierter Basispuffer: In diesen Fällen hängt der pH von PK abZu von schwacher Säure.
- Schwacher Basenpuffer und konjugierte Säure: In diesen Fällen hängt der pH von PK abB schwach.
- Polyprotische Säuresalzpuffer: In einigen Fällen sind sowohl die Rolle der schwachen Säure als auch ihre konjugierte Base beide Salze aus der partiellen Neutralisation einer Säure mit mehreren Protonen wie Schwefelsäure oder Phosphor.
Nach seinem letzten pH -Wert:
Abhängig von der Säure oder der Grundkonstante kann eine Pufferlösung den pH -Wert um verschiedene pH -Bereiche regulieren, was zu drei Arten von Puffer führt:
- Säurepuffer: Sind diejenigen, die den pH -Wert um die Werte von weniger als 7 regulieren. Sie werden mit schwachen Säuren hergestellt, deren PKZu weniger als 7 oder mit schwachen Basen sein, deren PKB mehr als 7 sein.
- Neutrale Puffer: Sind diejenigen, die den pH um 7 regulieren. Sie bestehen normalerweise aus schwachen Säuren oder Basen mit einem PKZu oder eine PKB nahe 7.
- Alkalische Puffer: Sind diejenigen, die den pH -Wert um Werte von mehr als 7 regulieren. Sie werden mit schwachen Säuren hergestellt, deren PKZu mehr als 7 oder mit schwachen Basen sein, deren PKB ist weniger als 7.
Beispiele für Puffer oder Dämpfungslösungen
Essigsäurepuffer/Natriumacetat
Dies ist ein Puffer einer schwachen Säure (Essigsäure) und ein Salz seiner konjugierten Base (Natriumacetat). Das Gleichgewicht und seine Gleichgewichtskonstante sind:
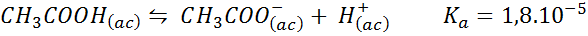
Dieser Puffer reguliert den pH -Wert um 4.74.
Ammoniakpuffer/Ammoniumchlorid
Dies ist ein schwacher Basenpuffer (Ammoniak oder Ammoniumhydroxid) und ein Salz seiner konjugierten Säure (Ammoniumchlorid). Das Gleichgewicht und seine Gleichgewichtskonstante sind:
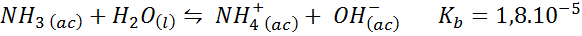
Dies ist ein alkalischer Puffer, der den pH -Wert umsetzt 9.26.
Bisulfat/Sulfatpuffer
In diesem Fall spielt das Bisulfation das Papier von schwacher Säure, dessen konjugierte Base das Sulfation ist. Das Gleichgewicht ist:
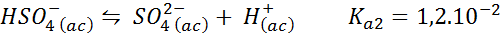
Dies ist eine Säure -Daming -Lösung, die den pH -Wert umsetzt 3.05.
Kohlensäure/Bicarbonat -Puffer
Dies ist eines der wichtigsten pH -Regulierungssysteme in unserem Blut. Die Reaktion ist: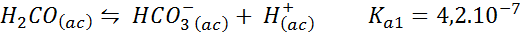
Dieser Puffer reguliert den pH -Wert um 6.38.
Dihydrogenpufferphosphat/Wasserstoffphosphat
Dies ist eines der am häufigsten verwendeten pH -Regulationssysteme in Biologie und Biochemie, da es ermöglicht. Die Reaktion ist:
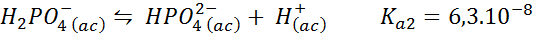
Dieser Puffer reguliert den pH -Wert um 7.20.

