Quantentabelle
- 3182
- 954
- René Riediger
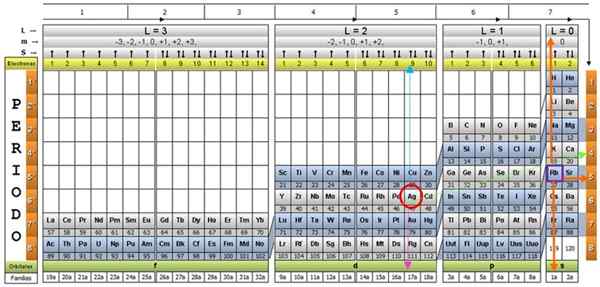
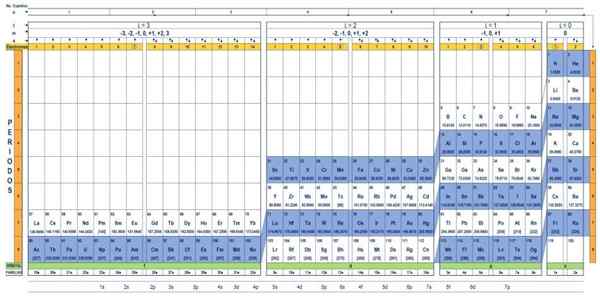 Die Quantentabelle der Elemente. Quelle: unam.
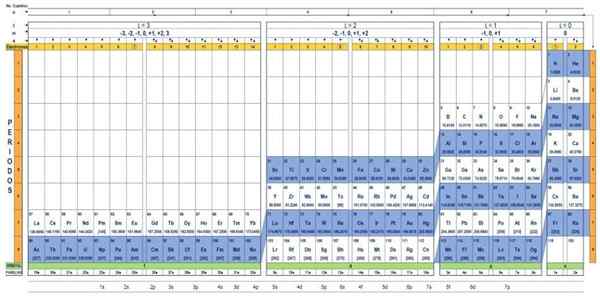
Die Quantentabelle der Elemente. Quelle: unam. Was ist die Quantentabelle??
Der Quantentabelle Es ist eine Möglichkeit, die chemischen Elemente zu organisieren, um den Satz von Quantenzahlen leicht zu bestimmen, die jede von ihnen charakterisieren.
Wissenschaftler haben festgestellt, dass es in der Natur aller Elemente bestimmte Muster gibt. Unter diesen Mustern sind Quantenzahlen, vier einfache Zahlen, die die elektronische Konfiguration jedes Elements beschreiben.
Quantenzahlen entstehen natürlich aus dem mechanisch-mechanischen Modell des Atoms und werden durch Buchstaben bezeichnet: n, ℓ, mℓ und s. Sie beschreiben den Energiestatus von Elektronen im Atom jedes chemischen Elements.
Durch die herkömmliche Periodenverkehrstabelle und einige zusätzliche Werkzeuge ist es möglich, die elektronische Konfiguration des Atoms eines beliebigen Elements zu haben. Der Vorteil der Quantentabelle besteht darin, dass die Elemente so organisiert sind, dass ihre Quantenzahlen sofort sichtbar sind, ohne dass zahlreiche Berechnungen separat durchgeführt werden müssen.
Eigenschaften der Quantentabelle
Es gibt mehrere Quantentabellen -Designs. Das in der obige Abbildung gezeigte Modell enthält:
- Ein Kopfball mit vier Zeilen mit den Werten der vier Quantenzahlen N, ℓ, M und S sowie einer fünften Reihe in Gelb, die der Anzahl der Elektronen im äußersten Orbital entspricht.
- Der Körperkörper, der aus einem Raster besteht. Die folgende Zahl repräsentiert die Menge der Atomelektronen in einem grundlegenden Zustand.
- Unten, in der grünen Reihe gibt es vier Klassen, um die Elemente zu organisieren: die Orbitale S, P, D und F (von links nach rechts).
- Schließlich befindet sich unter der Orbitalreihe die Familie. Jede Spalte ist eine Familie, die von 1 bis 32 nummeriert ist. Zum Beispiel gehören die 1. und 2. Familien zur S -Klasse, Familien vom 3. bis 8a, gehören zur Klasse P usw.
Was ist die Quantentabelle für?
Die Quantentabelle ermittelt den Satz von Quantenzahlen, der ein Elektron aus dem Atom charakterisiert. Normalerweise sind diese Elektronen die der äußersten Schicht, da sie diejenigen sind, die das chemische Verhalten des Elements definieren.
Wie ist die Quantentabelle??
Die Quantentabelle ermöglicht es, die Quantenzahlen der Elektronen in der äußersten Schicht des Atoms leicht zu finden.
Beispiel 1
Um das Verfahren zu veranschaulichen, wird das Aluminiumelement als Beispiel angenommen, dessen Symbol für das ist. Der erste Schritt besteht darin, es in der Quantentabelle zu lokalisieren und mit a zu markieren roter Kreis:
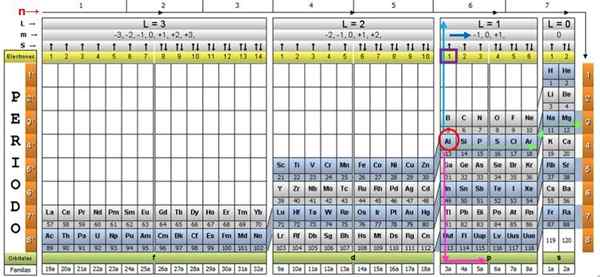
Schritt 1: Finden Sie n
Nachdem Sie das Element in der Tabelle lokalisiert haben, müssen Sie sich nach rechts durch die gleiche Reihe und die gleiche Farbe bewegen, bis Sie die orangefarbene Spalte erreichen, folgt der Straße des im Bild gezeigten grünen Pfeils.
Der Pfeil zeigt auf das markierte Feld mit Nummer 3, der Hauptquantennummer n:
n = 3
Schritt 2: Finden Sie ℓ
Um die sekundäre Quantenzahl zu bestimmen, wird der blaue vertikale Pfeil befolgt, was anzeigt:
ℓ = 1.
Schritt 3: Finden Sie M
Das externe Aluminiumelektron befindet sich in der Familie der Tischung P, wie in der grünen Reihe gelesen werden kann, auf die der rosa Pfeilspitze zeigt.
Darüber hinaus wird die Menge der Elektronen in der letzten Schicht in der gelben Reihe des Headers gelesen. Im Falle von Aluminium gibt es 1 Elektronen (im lila Quadrat hervorgehoben). Kombinieren Sie die obigen Ergebnisse, die Konfiguration der letzten Schicht lautet:
Kann Ihnen dienen: Galvanische Zelle: Teile, Wie funktioniert, Anwendungen, Beispiele3p1
Es ist bekannt, dass eine P -Schicht maximal 6 Elektronen unterstützt. Und die Zahl M nimmt einige der gesamten Werte - ℓ, ( - ℓ+1),… 0,… (+ℓ –1),+ℓ.
Wie in diesem Fall ℓ = 1 kann m dann –1, 0, 1 sein.
Diese Zahlen erscheinen in der Zeile des Headers, die M entspricht (siehe im Bild der Horizontaler Pfeil Blau). Die folgende Tabelle dient als Leitfaden, um zu wissen, was der Wert der Wahl ist, abhängig vom Fall:
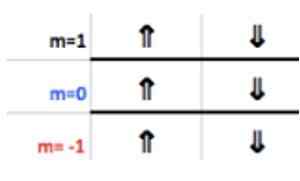
Da die letzte Aluminiumschicht 1 Elektron hat, entspricht die magnetische Quantenzahl
M = 1.
Schritt 4: Finden Sie S
Die Spinzahl S hat nur zwei Werte: +½ oder - ½. Wenn der Pfeil in der oberen Box angezeigt wird, wird er s = +½ gewählt und wenn er nach unten zeigt, dann s = - ½. Im Falle von Aluminium zeigt Elektron 1 also:
S = + ½.
Kurz gesagt, die Quantenzahlen des Elektrons der äußersten Aluminiumschicht zum Klang:
n = 3; ℓ = 1; M = 1, s = +½
Beispiel 2 (Ausnahmefälle)
Silber AG und etwa zwanzig weitere Elemente sind Ausnahmefälle, daher muss bei der Verwendung des Quantentabels mit ihnen darauf geachtet werden.
Wenn die vorherige Prozedur wiederholt wird, wird die AG als letztes Sub -Level auf dem 4D erhalten9.
Dies liegt daran, dass die vorhergesagte Konfiguration von La Plata nach Madelungsregel:
1s2 2s2 2 p6 3s2 3p6 4s2 3d10 4p6 5s2 4d9
In der Praxis folgt die AG jedoch nicht genau dieser Konfiguration, noch andere Elemente, deren letzte vorhergesagte Schicht 4D beträgt9, wie Kupfer und Gold unter anderem (wenden Sie sich an das Internet, um eine vollständige Liste von Elementen zu erhalten, die Madelungsregel nicht folgen).
Kann Ihnen dienen: MolealitätDie reale Konfiguration von AG ist:
1s2 2s2 2 p6 3s2 3p6 4s2 3d10 4p6 5s1 4d10
In dem ein Elektron der 5S -Schicht2 sprang in die 4D -Schicht9 um es zu vervollständigen. Auf diese Weise nimmt die Stabilität des Atoms zu. Daher ist der letzte Sub -Level wirklich:
5s1
Und seine Quantenzahlen wären diejenigen, die dem RB -Element entsprechen, die in einem lila Box gezeigt sind und orangefarbene Pfeile auf die verbleibenden Zahlen zeigen:
n = 5; ℓ = 0; M = 0; S = +½
 Überprüfung der Periodenzüchtertabelle, tatsächlich ist festgestellt, dass AG in Periode 5 ist, ein Merkmal, das durch die Hauptquantennummer N bestimmt wird.
Überprüfung der Periodenzüchtertabelle, tatsächlich ist festgestellt, dass AG in Periode 5 ist, ein Merkmal, das durch die Hauptquantennummer N bestimmt wird.
Unterschiede mit der Periodenzüchtertabelle
Beide Tabellen sind zwei Möglichkeiten, die chemischen Elemente nach den Eigenschaften ihrer Atome zu organisieren:
-In der Periodischabelle haben die in derselben Spalte gefundenen Elemente ähnliche chemische Eigenschaften. Zum Beispiel beginnt es mit der alkalischen Metallensäule links und endet die der edlen Gase nach rechts. Während in den Reihen die Elemente mit dem gleichen höheren Energieniveau sind.
-Die Quantentabelle hat eine stetige Disposition, die gemäß den Füllregeln ausgelegt ist. Daher müssen Sie die Schritte ausführen, um die Hauptquantenzahl, außer im Fall von Ausnahmen wie Silber, im Beispiel des vorherigen Abschnitts zu erhalten. Die Familien von Elementen in dieser Tabelle werden durch das obere Orbital in S, P, D oder F zusammenhängen.
Verweise
- Chang, R. 2013. Chemie. 11va. Auflage. McGraw Hill Education.
- Elektronische Konfiguration. Elektronische Konfiguration und Quantenzahlen. Abgerufen von: configUionectronica.com.
- Chemiehandbuch. Abgerufen von: DCB.Maschinenbau.Unam.mx.
- Offizielle Chemie. So einfach Quantenzahlen einfach. Abgerufen von: Chemiebeamter.com
- Triplenlace. Ausnahmen von der Regel von Madelung in der elektronischen Konfiguration chemischer Elemente. Abgerufen von: Triplenlace.com.

