Natriumthiosulfat (Na2s2O3)

- 882
- 100
- René Riediger
 Natriumthiosulfatsalze. Mit Lizenz
Natriumthiosulfatsalze. Mit Lizenz Was ist Natriumthiosulfat?
Er Natriumthiosulfat oder Natriumhyposulfit (NA2S2ENTWEDER3) Es ist ein wichtiges anorganisches Salz mit mehreren medizinischen Anwendungen. Es ist auch als Ihr Pentahydrat -Salz erhältlich (NA2S2ENTWEDER3.5H2ENTWEDER).
Es ist eine ionische Verbindung, die von zwei Natriumkationen gebildet wird (Na+) und die negativ belasteten Thiosulfatanionen (s)2ENTWEDER3-), in dem das zentrale Schwefelatom mit drei Sauerstoffatomen und einem anderen Schwefelatom (daher das Präfix -Tio) durch einfache und doppelte Bindungen mit Resonanzcharakter verbunden ist. Der Feststoff existiert in einer monoklinen kristallinen Struktur.
Natriumthiosulfat kann Heizschwefel mit einer wässrigen Natriumsulfitlösung oder einer wässrigen Natriumhydroxidlösung herstellen.
6naoh + 4s → na2S2ENTWEDER3 + 22S + 3H2ENTWEDER
Dies ist ein Medikament, das auf der Liste der wesentlichen Medikamente der Weltgesundheitsorganisation steht, die effektivsten und sichersten Medikamente, die in einem Gesundheitssystem benötigt werden.
Physikalische und chemische Eigenschaften
- Natriumthiosulfat hat ein Molekulargewicht von 158,11 g/mol für wasserfreie Form und 248,18 g/mol für die Pentahydratform.
- Präsentiert eine Dichte von 1.667 g/ml.
- Natriumthiosulfat ist ein farbloser monokliner Kristall ohne charakteristisches Aroma. Dieser Feststoff ist aus dem Ausblühen, was bedeutet, dass er selbst durch Verlust des Kristallisationswassers auf Staub reduziert werden kann, wenn er Luft ausgesetzt ist.
- Die Verbindung hat einen Schmelzpunkt von 48 ° C für die Pentahydratform und beginnt sich von 100 ° C zu zersetzen.
- Dann ein2S2ENTWEDER3 Es ist sehr löslich in Wasser und kann 70 Gramm pro 100 Milliliter Lösungsmittel auflösen. Die Verbindung ist in Ethanol praktisch unlöslich.
Kann Ihnen dienen: Absorptionsspektrum- Natriumthiosulfat ist ein neutrales Salz, das leicht in Wasser disoziiert, um Natrium- und Thiosulfationen zu ergeben. N / A2S2ENTWEDER3 Es ist ein stabiler Feststoff unter normalen Bedingungen, zersetzt sich jedoch beim Erhitzen, um Natriumsulfat und Natriumpolysulfid zu ergeben:
4na2S2ENTWEDER3 → 3na2SW4 + N / A2S5
- Es bricht auch zusammen, wenn es mit verdünnten Säuren behandelt wird, um Schwefel und Schwefeldioxid (Taktreaktion genannt) zu ergeben:
N / A2S2ENTWEDER3 + 2HCl → 2naCl + S + SO2 + H₂o
- Stöchiometrisch reagiert (in äquimolaren Größen) mit wässrigen Jodlösungen, sodass es in Laboratorien für Jodgrade häufig verwendet wird.
Reaktivität und Gefahren
Natriumthiosulfat ist kein giftiges Material und wird für medizinische Zwecke verwendet. Wenn es sich jedoch zersetzt, erzeugt es jedoch giftige Schwefeloxid -Dämpfe, die zu Reizungen in den Augen, Haut und Schleimhäuten führen können.
Die Verbindung kann die Augen, die Haut und die Atemwege reizen. Die Substanz ist für die Lungen und die Schleimhäute giftig. Wiederholte oder längere Exposition gegenüber der Substanz kann diese Organe beschädigen.
Wenn die Verbindung mit den Augen in Kontakt kommt, müssen die Kontaktlinsen überprüft und entfernt werden, um sie zu tragen. Die Augen mit viel Wasser sollten sofort mindestens 15 Minuten mit kaltem Wasser gewaschen werden.
Im Hautkontakt muss der betroffene Bereich mindestens 15 Minuten lang ausgespült werden, während die kontaminierten Kleidung und Schuhe entfernt werden.
Sie müssen die Haut abdecken, die mit einem Emollient gereizt ist. Waschen Sie Kleidung und Schuhe, bevor Sie sie wieder benutzen. Wenn der Kontakt ernst ist, waschen Sie mit einer Desinfektionsseife und bedecken Sie die mit einer antibakterielle Creme kontaminierte Haut.
Kann Ihnen dienen: Sauerstoff: Eigenschaften, Struktur, Risiken, verwendetIm Inhalation muss das Opfer an einen neuen Ort übertragen werden. Wenn Sie nicht atmen, wird künstliche Atmung verabreicht. Wenn das Atmen schwierig ist, muss Sauerstoff bereitgestellt werden.
Wenn die Verbindung aufgenommen wird, sollte Erbrechen nicht induziert werden, es sei denn, das medizinische Personal gibt es an. Lösen Sie enge Kleidung wie Hemdhals, Gürtel oder Krawatte.
In allen Fällen muss eine sofortige medizinische Versorgung erhalten werden.
Anwendungen
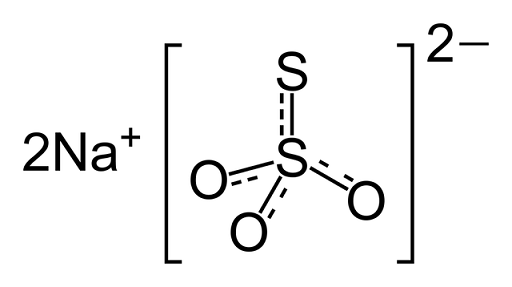 Chemische Struktur von Natriumthiosulfat
Chemische Struktur von Natriumthiosulfat Medizin
- Natriumthiosulfat kann verwendet werden, um einige der Nebenwirkungen des Cisplatins (einer Krebsmedizin) zu reduzieren.
- Es wird zur Behandlung von Extravasation während der Chemotherapie verwendet. Natriumthiosulfat verhindert die Alkylierung und Zerstörung des Gewebes und liefert ein Substrat für gemietete Wirkstoffe, die in subkutane Gewebe eingedrungen sind.
- Es wird auch mit einem anderen Medikament zur Notfallbehandlung der Cyanidvergiftung verwendet.
In dieser Behandlung wird Natriumnitrit intravenös injiziert, um Hämoglobin zu produzieren, das mit dem Cyanid -Ion kombiniert wird, wodurch es vorübergehend in die Cianemetoglobinform umdreht. Anschließend wird Natriumthiosulfat injiziert.
- Es dient als Substrat für das Rodanasa -Enzym, das die Cyanidumwandlung in das viel weniger giftige Tiocianat katalysiert, das im Urin ausgeschieden ist.
- Es wird auch zur Behandlung der Kalkifilaxis bei Menschen bei Hämodialyse mit terminaler Nierenerkrankung verwendet. Anscheinend gibt es ein nicht vollständig verstandenes Phänomen, bei dem bei einigen Patienten eine schwere metabolische Azidose verursacht.
Iodometrie
- Natriumthiosulfat reagiert stöchiometrisch mit Jod, um Jodid gemäß der Reaktion zu geben:
Kann Ihnen dienen: Ketone: Typen, Eigenschaften, Nomenklatur, Verwendungen, Beispiele22S2ENTWEDER3 + I2 → s4ENTWEDER62– + 2i- -
Diese Eigenschaft macht die Verbindung, die als Titel bei der Bestimmung von Jod verwendet wird.
- Diese besondere Verwendung kann festgelegt werden, um den Sauerstoffgehalt des Wassers durch eine lange Reihe von Reaktionen im Winkler -Test auf gelöstem Sauerstoff zu messen.
- Es wird auch in der volumetrischen Schätzung der Konzentrationen bestimmter Verbindungen in Lösung (z.
Wasser Wasser
- Natriumthiosulfat wird verwendet, um Wasser zu offenbaren.
Die Reduktionsreaktion ist analog zur Iodinreduktionsreaktion, das Thiosulfat reduziert den Hypochlorit (Wirkstoff im Bleichmittel) und dadurch oxidiert sie zu Sulfat. Die vollständige Reaktion ist:
4naclo + na2S2ENTWEDER3 + 2naoh → 4nacl + 2na2SW4 + H2ENTWEDER
Goldgewinnung
Natriumthiosulfat ist eine Komponente. Es bildet jedoch einen starken löslichen Komplex mit Goldionen (i), [Au (s)2ENTWEDER3)2]3-.
Der Vorteil dieses Ansatzes besteht.
Verweise
- HSDB: Natriumthiosulfat. Von Toxnet wiederhergestellt.NLM.NIH.Regierung.
- Sicherheitsdatenblatt Natrium Thiosulfat wasserfreies Material. Von Sciencelab geborgen.com.

