Toriostruktur, Eigenschaften, erhalten, verwendet, verwendet

- 1005
- 134
- Tizian Liebich
Er Torio Es ist ein metallisch. Es hat eine Atomzahl von 90 und ein Atomgewicht von 232 g/mol. Torioverbindungen enthalten es normalerweise mit Oxidationszahl +4 (TH4+).
Die Torio -Dioxidverbindung, tho2, Es ist industriell als Toria bekannt und wird in den meisten Toriumanwendungen verwendet, die durch die chemische Verbindung mit dem größten Schmelzpunkt gekennzeichnet sind (3.300 ºC).
 Metallic Thorium -Probe in einer Glasblase unter Argon gespeichert. Die schwärzliche Beschichtung ist auf sein Oxid zurückzuführen. Quelle: Alchemist-HP (Talk) (www.Pse-Mendelejew.de) / fals
Metallic Thorium -Probe in einer Glasblase unter Argon gespeichert. Die schwärzliche Beschichtung ist auf sein Oxid zurückzuführen. Quelle: Alchemist-HP (Talk) (www.Pse-Mendelejew.de) / fals Der Torio wurde 1828 von Mortar Thrane Esmark entdeckt, der auf der norwegischen Insel Løvøya ein schwarzes Mineral fand. Esmark lieferte das Mineral an Jöns Jacob Berzelius, der ihn analysierte, ein unbekanntes Metall in ihm zu finden.
Er nannte das schwarze Mineral als Torita (Thorita) zu Ehren des skandinavischen Gottes Thor Thor. Inzwischen hieß das unbekannte Metall Torio (Thorium). Der radioaktive Charakter des Thoriums wurde von Anton Edward Van Arkel und Jan Hendrik de Boer und unabhängig von Pierre Curie und Marie Curie gegründet.
[TOC]
Toriumeigenschaften
Physisch
Das Thorium ist ein radioaktives, helles, mäßig hartes, silberndes, duktiles und formbares weißes Metall, das sehr langsam in der Luft nimmt, grau und später schwarz wird. Es gehört zur Gruppe der Actiniden und identifiziert sich mit der Atomzahl 90 und einem Atomgewicht von 232 g/mol.
Radioaktivität
Der Torio-232 (232Th90) macht mehr als 99% des gesamten Thoriumelements aus, das im Erdkortex vorhanden ist. Es kann angenommen werden, dass es ein stabiles Isotop ist, obwohl es radioaktiv ist, da sein halbes Leben 1 ist.405 x 1010 Jahre. Radioaktiv durch Emission von α- und β -Partikeln und γ -Strahlung abnimmt.
Der Torio-232 wird in das Radio-268 (268Ra88) durch Ausgabe eines Alpha -Partikels, das aus zwei Protonen und zwei Neutronen besteht. Das Thorium kann eine Reihe von radioaktiven Zerfällen erleiden, bis es zu einem stabilen Element wird: Lead-208.
Kann Ihnen dienen: Bleichlorid: Eigenschaften, Struktur, verwendetDer Torio-232 kann Neutronen fangen, um sich in das radioaktive Uran-233-Element zu verwandeln, wodurch β-Typ-Strahlung emittiert wird. Uran dagegen wird in Kernreaktoren für die Energieerzeugung eingesetzt.
Reaktivität
Das Thorium ist ein elektropositives und hochreaktives Metall. Es oxidiert sehr langsam in der Luft, obwohl nach einigen Monaten Korrosion auftreten kann. Wenn es in der Luft erhitzt wird, wird es eingeschaltet und ein leuchtendes weißes Licht ausstrahlt, während die Herstellung von Torio -Dioxid, tho2.
Unter Standardtemperatur- und Druckbedingungen wird das Thorium langsam durch Wasser angegriffen. Ebenso wird das Thorium nicht in den meisten häufigen Säuren gelöst, mit Ausnahme von Salzsäure, wo es einen schwarzen, unlöslichen Rückstand auflöst.
Es wird auch in konzentrierter Salpetersäure mit einer geringen Menge katalytischer oder fluorosylikatem Fluorid gelöst. Das Thorium ist ein pyrophorisches Metall: Wenn es pulverisiert wird, kann es spontan entzünden.
Struktur
Torio -Atome bilden eine Kubikstruktur, die bei Raumtemperatur auf den Gesichtern (FCC) zentriert ist. Wenn es über 1360 ° C erhitzt wird, erleidet das Glas einen Übergang zur kubischen Phase, die auf dem Körper (BCC) mit niedrigerer Dichte zentriert ist. In der Zwischenzeit erlangt das Thorium unter hohen Drücken (100 GPa oder mehr) eine dichte tetragonale Struktur, die auf dem Körper zentriert ist (BCT).
Elektronische Konfiguration
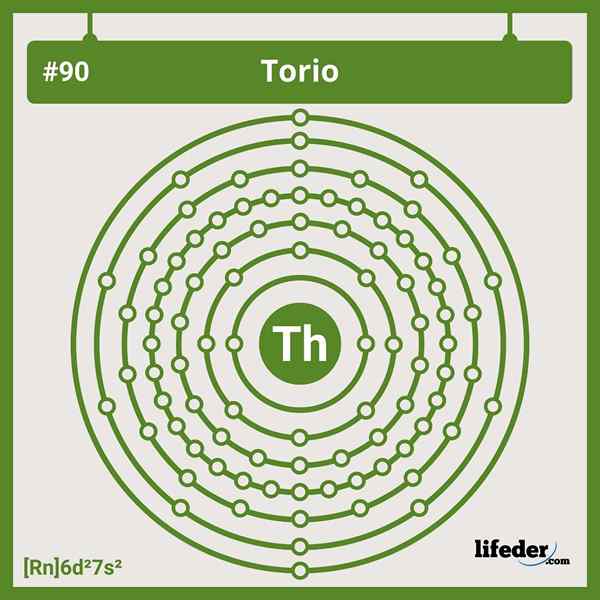 Elektronische Toriumeinstellungen
Elektronische Toriumeinstellungen Die abgekürzte elektronische Konfiguration für das Thorium lautet wie folgt:
[Rn] 6d2 7s2
Verlieren der vier Valencia -Elektronen verwandeln sich in das Kationen4+. Beachten Sie, dass es trotz der Schauspielerei im Gegensatz zu den anderen Aktiniden die Elektronen in seinen 5F -Orbitalen fehlen.
Kann Ihnen dienen: VerbreitungsphaseErhalten
Das Hauptmineral, das zum Erhalten des Thoriums verwendet wird, ist der Monacit. Der erste Schritt ist seine Trennung von seiner Hauptablagerung: die Pegmatita. Alkalinotal -Metalle Carbonate werden durch Reaktion ihrer Fragmente mit Wasserstoffchlorid aus dem Pegmatit eliminiert.
Die resultierenden Fragmente werden kalkiniert und filtriert und dann einer magnetischen Trennung unterzogen. Somit wird ein sandiges Material von Monacita erhalten. Dieser Sand wird einer 93%igen Schwefelsäureverdauung, bei einer Temperatur von 210 bis 230 ° C und mehreren Stunden ausgesetzt. Die gebildete Säurelösung wird später das zehnfache Volumen mit Wasser verdünnt.
Monacitas Überreste sinken auf den Boden, während das Thorium und die anderen Elemente der Seltenen Erde in der Säurevorbereitung schwimmen. PH bis 1 wird eingestellt.3, der die Ausfällung des Thoriums als Phosphat erzeugt, während der Rest des seltenen Landes in Suspension in Lösung bleibt.
Derzeit werden die Trennung und Reinigung unter Verwendung von flüssigen Lösungsmitteln durchgeführt, z. B. Tributphosphat in queroseno.
Torio -Metall kann in kommerziellen Größen durch metallothermische Reduktion in Totrafluoruro de Torio (THF) auftreten4) und Torio Dioxid (tho2) oder durch Elektrolyse von Thoriumtetrachlorid (THCL4).
Anwendungen
Das Thorium hat viele Anwendungen, von denen viele seit den 1950er Jahren verworfen wurden, weil sein radioaktiver Charakter ein Gesundheitsrisiko darstellt.
Industrielle
Legierungen
Das Thorium wurde mit dem Wolfram als Elektrode im TIG -Schweißen (Wolfram -Inertgas) legiert, was 2% der Legierung ausmachte.
In kleinen Mengen wurde Torio zu Wolframfilamenten gegeben. Wolfram-Torio-Drähte wurden in elektronischen Röhrchen und in den Elektroden der Röntgen- und Gleichrichterrohre verwendet.
Torio -Dioxid wurde im Wolfram -Lichtbogenschweißen verwendet, da die Wolframwiderstand gegen hohe Temperaturen von Metallelektroden zunimmt. Es wurde jedoch in dieser Anwendung durch Umfangsherren, Cerio oder Lantano -Oxide ersetzt.
Kann Ihnen dienen: Woher kommt Plastik?? Geschichte und TypenBlitz
Totrafluoruro de Torio hingegen wurde als Material verwendet, um die Reflexe in multicapa optischen Beschichtungen zu reduzieren, die mit einer Wellenlänge zwischen 0 transparent sind.350 bis 1.2 µm. Torio Salz wurde jedoch in dieser Verwendung durch den Tetrafluoruro de Lantano ersetzt.
Torio -Dioxid wurde bei der Lichtbeleuchtung verwendet, um ein brillantes Licht zu emittieren, das sichtbarem Licht entspricht. Obwohl das Thorium in dieser Anwendung noch verwendet wird, wurde es teilweise durch das ITE ersetzt.
Feuerfeste Materialien
Das Thorium wurde auch zur Ausarbeitung von feuerfesten Materialien für die metallurgische Industrie und in Keramikkrisolen für Lehr- und Forschungslabors eingesetzt.
Kernreaktoren
Der Torio-232 wird in Kernreaktoren eingesetzt, um Zeitlupe-Neutronen zu fangen, da dies in Uranium-233 umgewandelt wird. Dieses radioaktive Element wird physisch und wird für die Energieerzeugung verwendet.
Die Entwicklung von Kernreaktoren basierend auf dem Torio-32 war langsam und schuf den ersten Reaktor mit diesem Merkmal im indischen Point Energy Center in Buchanan USA, im Jahr 1962. Torio-232 Kernreaktoren emittieren kein Plutonium, was sie weniger Schadstoffe macht.
Verweise
- Shiver & Atkins. (2008). Anorganische Chemie. (vierte Edition). Mc Graw Hill.
- Wikipedia. (2020). Thorium. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologieinformationen (2020). Thorium. Pubchem Comunund -Zusammenfassung für CID 23974. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- DR. Doug Stewart. (2020). THORIUM -Element -Fakten. Erholt von: Chemicoolool.com
- Die Herausgeber von Enyclopaedia Britannica. (2020). Thorium. Erholt von: Britannica.com
- Lentech b.V. (2020). Thorium. Erholt von: lentech.com
- Rachel Ross. (1. März 2017). Fakten über Thorium. Erholt von: Livescience.com
- Advameg. (2020). Thorium. Erholt von: ChemistryExplaed.com

