Verflüchtigung

- 4125
- 188
- Lewis Holzner
 Wenn Wasser in einer Platte erhitzt wird, bis Dampf auftritt. Mit Lizenz
Wenn Wasser in einer Platte erhitzt wird, bis Dampf auftritt. Mit Lizenz Was ist Verflüchtigung?
Der Verflüchtigung Es ist der Prozess, eine Chemikalie eines flüssigen oder festen Zustands in einen gasförmigen oder Dampf umzuwandeln. Andere Begriffe, die zur Beschreibung desselben Prozesses verwendet werden, sind Verdampfung, Destillation und Sublimation.
Eine Substanz kann oft durch Verflüchtigung von einer anderen getrennt werden und durch Dampfkondensation gewonnen werden.
Die Substanz kann schneller verwandelt werden und entweder erhitzt, um ihren Dampfdruck zu erhöhen, oder durch Dämpfen unter Verwendung eines inerten Gasstroms oder einer Vakuumpumpe.
Zu den Heizverfahren gehören die Verflüchtigung von Wasser, Quecksilber oder Arsentrichlorid, um diese Substanzen von den Interferenzelementen zu trennen.
Manchmal werden chemische Reaktionen verwendet, um flüchtige Produkte wie bei der Freisetzung von Kohlendioxid aus Carbonaten zu produzieren, Ammoniak im Kjeldahl -Verfahren zur Bestimmung von Stickstoff und Schwefeldioxid bei der Bestimmung von Stahlschwefel.
Volatilisierungsmethoden sind im Allgemeinen durch große Einfachheit und einfache Funktionsweise gekennzeichnet, außer wenn sie korrosionsbeständig oder Materialien benötigt werden.
Dampfdruckvolatilisation
Wenn man weiß, dass die kochende Wassertemperatur bei 100 ° C liegt, ist es relevant zu fragen, warum Regenwasser verdunstet. Wenn es bei 100 ° C ist, sollte es uns Wärme geben.
Es lohnt sich auch zu fragen, was das charakteristische Aroma Alkohol, Essig, Holz oder Plastik gibt.
Die Person, die für all dies verantwortlich ist. Auch der Teildruck der Substanz in der Atmosphäre auf dem Feststoff oder der Flüssigkeit.
Der Dampfdruck ist ein Maß für die Tendenz eines Materials, der in den gasförmigen oder Dampfzustand geändert wird, dh ein Maß für die Substanzvolatilität.
Es kann Ihnen dienen: Kohlenstoffdisulfid (CS2): Struktur, Eigenschaften, Verwendungen, RisikenMit zunehmender Dampfdruck.
Der Dampfdruck nimmt mit der Temperatur zu. Die Temperatur, bei der der Dampfdruck auf der Oberfläche einer Flüssigkeit dem durch die Umgebung ausgeübten Druck entspricht.
Der Dampfdruck hängt von dem in Lösung gelösten gelösten gelösten gelösten gelösten Stoffdruck ab (es handelt sich um eine koligative Eigenschaft). Auf der Oberfläche der Lösung (lufttiefe Grenzfläche) verdampfen die oberflächlichsten Moleküle tendenziell, zwischen Phasen auszutauschen und Dampfdruck zu erzeugen.
Das Vorhandensein von gelösten Stoff verringert die Anzahl der Lösungsmittelmoleküle an der Grenzfläche und verringert den Dampfdruck.
Die Änderung des Dampfdrucks kann mit dem Raault -Gesetz für nicht -volatile gelöste gelöste berechnet werden, die angegeben werden durch:
(1) Wenn p1 der Dampfdruck nach Zugabe des gelösten Stoffes ist, ist x1 der molare Anteil des gelösten Stoffes und P ° der Dampfdruck des reinen Lösungsmittels.
Wenn p1 der Dampfdruck nach Zugabe des gelösten Stoffes ist, ist x1 der molare Anteil des gelösten Stoffes und P ° der Dampfdruck des reinen Lösungsmittels.
Wenn die Summe der molaren Fraktionen des gelösten Stoffes und des Lösungsmittels gleich 1 ist, haben wir:
(2)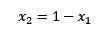
Wobei x2 der Molfraktion des Lösungsmittels ist. Wenn wir beide Seiten der Gleichung mit P ° multiplizieren, bleibt es:
(3)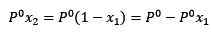
Ersetzen von (1) in (3) bleibt:
(4)
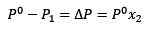
Dies ist die Variation des Dampfdrucks, wenn sich ein gelöster Stoff auflöst.
Gravimetrische Analyse
Die gravimetrische Analyse ist eine Klasse von Labortechniken.
Der Chemiker, den wir quantifizieren möchten, wird manchmal als Analyt bezeichnet. Wir könnten die gravimetrische Analyse verwenden, um Fragen zu beantworten wie:
Kann Ihnen dienen: Metallmineralien- Was ist die Konzentration des Analyten in einer Lösung??
- Wie rein ist unsere Probe? Die Probe hier könnte ein fester oder in Lösung sein.
Es gibt zwei häufige Arten von gravimetrischer Analyse. Beide beinhalten die Änderung der Analytphase, um sie vom Rest einer Mischung zu trennen, was zu einer Änderung des Teigs führt.
Eine dieser Methoden ist die Niederschlagsgravimetrie, aber diejenigen, die uns wirklich interessiert, ist die Verflüchtigung der Gravimetrie.
Die Valatilisation -Gravimetrie basiert auf thermischer oder chemischer Probe und misst die resultierende Änderung seiner Masse.
Alternativ können wir ein flüchtiges Produkt der Zersetzung fangen und wiegen. Da die Freisetzung einer flüchtigen Spezies ein wesentlicher Bestandteil dieser Methoden ist, klassifizieren wir sie gemeinsam als gravimetrische Valatilisierungsanalysemethoden.
Gravimetrische Analyseprobleme sind einfach Stöchiometrieprobleme mit einigen zusätzlichen Schritten.
Um eine stöchiometrische Berechnung durchzuführen, benötigen wir die Koeffizienten der ausgewogenen chemischen Gleichung.
Wenn beispielsweise eine Probe Verunreinigungen von dihydratisiertem Barium (BACL) enthält2● H₂o) können Sie die Menge an Verunreinigungen erhalten, die die Probe erhitzt, um das Wasser zu verdampfen.
Der Massenunterschied zwischen der ursprünglichen Probe und der erhitzten Probe ergibt uns in Gramm die Menge an Wasser, die im Bariumchlorid enthalten ist.
Mit einer einfachen stöchiometrischen Berechnung wird die Menge an Verunreinigungen der Probe erhalten.
Fraktionierte Destillation
Die fraktionale Destillation ist ein Prozess, durch den die Komponenten eines flüssigen Gemisches in verschiedene Teile (als Brüche genannt) gemäß ihren verschiedenen Siedepunkten unterteilt werden.
Die Volatilitätsdifferenz der Verbindungen der Mischung spielt eine grundlegende Rolle bei der Trennung.
Kann Ihnen dienen: OktettregelFraktionelle Destillation wird verwendet, um Chemikalien zu reinigen und auch Gemische zu trennen und ihre Komponenten zu erhalten. Es wird als Labortechnik und in der Branche verwendet, wo der Prozess eine große kommerzielle Bedeutung hat.
Die Dämpfe einer kochenden Lösung werden entlang einer hohen Säule übergeben, die als Unterteilungssäule bezeichnet wird.
Die Säule ist mit Plastik- oder Glasperlen gepackt, um die Trennung zu verbessern, und bietet mehr Oberfläche für Kondensation und Verdunstung.
Die Säulentemperatur nimmt allmählich entlang ihrer Länge ab. Die Komponenten mit einem höheren Siedepunkt sind in der Säule kondensiert und kehren zur Lösung zurück.
Die unteren Siedepunktkomponenten (flüchtiger) gehen durch die Säule und werden in der Nähe der Oberseite gesammelt.
Theoretisch verbessert mehr Perlen oder Platten die Trennung, aber die Zugabe von Platten erhöht auch die Zeit und Energie, die für die Abschluss einer Destillation erforderlich sind.
Spannungsbeispiele
- Ein Block Trockeneis in Kontakt mit einem Luftausbruch. Die Luft beginnt mit dem Verflüchtigenungsprozess und das Eis verdunstet: Es geht vom Festkörper bis zum Soda über.
- Wenn Wasser oder eine andere Substanz gekocht ist: Wärme erzeugt Dampf und somit geht Wasser vom flüssigen Zustand zum Gas über.
- Die Naphthalinpillen, die sich allmählich verschlechtern und vom Festkörper bis zum Soda übergehen.
- Wenn fester Schwefel hohen Temperaturen ausgesetzt ist, wird er zu toxischen Gasen. Das heißt, es geht von fest zu gasförmig.
- Aromatisierungspillen: Sie haben den gleichen Prozess wie Naphthalinpillen, verschlechtern sich allmählich und werden Gas, Geruch und harmlos.
Verweise
- Druckdefinition Dampf. Von Thakedco erholt.com.
- Dampfdruck. Von Britannica geborgen.com.

