Schwefeloxid
- 1001
- 69
- Joe Hartwig
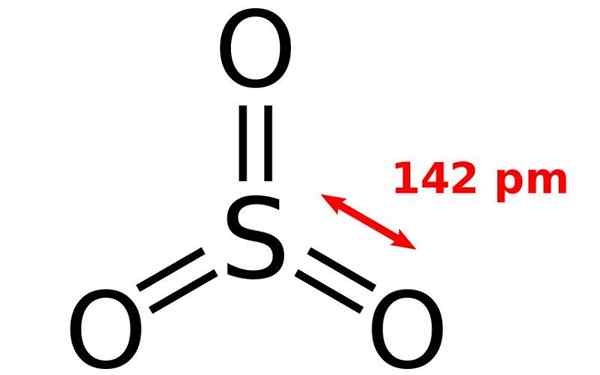
 Chemische Struktur des Schwefeloxidmoleküls. Quelle: Joel Holdsworth, Wikimedia Commons
Chemische Struktur des Schwefeloxidmoleküls. Quelle: Joel Holdsworth, Wikimedia Commons Was ist Schwefeloxid?
Er Schwefeloxid (Vi), auch als Schwefel- oder Schwefelanhydridtrioxid bekannt, ist eine chemische Verbindung der Formel S3, Das ist unter normalen Bedingungen ein farbloser und faseriger Feststoff, und bei 25 ° C und 1 atm ist ein starkes Verschmutzungsmittel, das für sauren Regen verantwortlich ist.
Schwefeltrioxid wird durch Oxidation von Schwefeloxid erzeugt.
Bisher jedoch die einzige reine Schwefel -Trioxidpräparation aus Gasen, die enthalten3 Verdünnt war es ein Verfahren in einer Pilotanlagenskala, die eine kryoskopische Kondensation impliziert.
Das übliche Verfahren impliziert stattdessen Öldestillation. Die für die Öldestillation erforderliche Wärme wird bequemer durch heißes Kontaktgas aus der damit verbundenen Schwefelsäure -Pflanze geliefert.
Es kann im Labor durch Erhitzen von Schwefelsäure des Rauchens vorbereitet und in einem gekühlten Empfänger sublimiert werden. Wenn der Dampf über 27 ° C kondensiert ist, wird die Gammastform als Flüssigkeit erhalten.
Wenn der Dampf unter 27 ° C und in Gegenwart einer Feuchtigkeitslinie kondensiert wird, wird eine Mischung der drei Formen erhalten. Die 3 Formen können durch fraktionierte Destillation getrennt werden.
Das Verbrennen fossiler Brennstoffe ist die Ursache für sein Aussehen in der Atmosphäre. Dies ist die wichtigste anthropogene Ursache.
Physikalische und chemische Eigenschaften von Schwefeloxid
- Schwefeltrioxid ist wie weiße Nadeln geformt, die zu Rauch in der Luft werden. Sie begegnen häufig Inhibitoren, um eine Polymerisation zu vermeiden.
Kann Ihnen dienen: Renio: Entdeckung, Eigenschaften, Struktur, verwendet- Sein Molekulargewicht beträgt 80.066 g/mol, seine Dichte beträgt 1,92 g/cm³ g/ml und die Fusions- und Siedepunkte betragen 16,8 ° C bzw. 44,7 ° C.
- Die Verbindung wird mit Wasser mit explosiver Kraft kombiniert und bildet aufgrund ihrer Säure Schwefelsäure. Carboniza -Schwefel -Trioxid organische Substanzen.
- Schwefeltrioxid absorbiert Feuchtigkeit schnell und emittiert dichte weiße Dämpfe. Schwefelsäure -Trioxidlösungen werden als Raucherschwefelsäure oder Öl bezeichnet.
- Die Schwefeltrioxidreaktion und der Sauerstoffdiffuorid sind sehr kräftig und Explosionen werden erzeugt, wenn die Reaktion in Abwesenheit eines Lösungsmittels durchgeführt wird.
- Die Reaktion überschüssiger Schwefeltrioxid mit Tetrafluorethylen verursacht die explosive Zersetzung von Carbonylfluorid und Schwefeldioxid.
- Die Reaktion der wasserfreien Perchlorsäure mit Schwefeltrioxid ist gewalttätig und wird von der Entwicklung beträchtlicher Wärme begleitet. Flüssigschwefeltrioxid reagiert heftig mit Nitrilchlorid, sogar 75 ° C.
- Die Schwefeltrioxidreaktion und das Bleioxid verursachen weiße Lumineszenz. Die Kombination von Jod, Pyridin, Schwefel und Formamid -Trioxid entwickelte nach mehreren Monaten ein Gas bei der Druckaufnahme.
Dies ist auf die langsame Bildung von Schwefelsäure, äußerem Wasser oder Dehydratisierung von Wasserstoffcyanidformamid zurückzuführen.
Risiken
Schwefeltrioxid ist eine stabile Verbindung, die mit organischen Materialien, fein pulverisierten Metallen, Basen, Wasser, Cyaniden und einer Vielzahl anderer Chemikalien nicht kompatibel ist.
Die Substanz ist ein starkes Oxidationsmittel und reagiert heftig mit brennbaren Materialien und Organisatoren und organischen Verbindungen, die eine Brand- und Explosionsgefahr verursachen.
Kann Ihnen dienen: Natriumoxalat (Na2C2O4): Struktur, Eigenschaften, Verwendungsmöglichkeiten, RisikenReagiert heftig mit Naswasser und Luft, um Schwefelsäure zu produzieren. Die Lösung in Wasser ist eine starke Säure, sie reagiert heftig mit Basen und korrosiven Metallen und bildet brennbares / explosives Gas.
Die Verbindung ist für Metalle und Gewebe korrosiv. Verursacht Verbrennungen in Augen und Haut. Die Aufnahme führt zu schweren Verbrennungen im Mund, der Speiseröhre und im Magen. Der Dampf ist durch Inhalation sehr giftig.
Bei Augenkontakt müssen Sie überprüfen, ob Kontaktlinsen verwendet werden, und sie sofort entfernen. Die Augen sollten mindestens 15 Minuten lang mit fließendem Wasser gespült werden und die Augenlider offen halten. Kaltes Wasser kann verwendet werden, ohne Augensalbe aufzutragen.
Wenn die Chemikalie mit der Kleidung in Kontakt kommt, behalten Sie sie so schnell wie möglich und schützen Sie ihre eigenen Hände und Körper. Legen Sie das Opfer unter eine Sicherheitsdusche.
Wenn sich die Chemikalie in der exponierten Haut des Opfers wie den Händen ansammelt, wird die mit fließende Wasser und nicht abrasive Seife kontaminierte Haut sanft gewaschen und vorsichtig. Kaltes Wasser kann verwendet werden. Wenn Reizungen bestehen, suchen Sie medizinische Hilfe auf. Waschen Sie kontaminierte Kleidung, bevor Sie sie wieder benutzen.
Im Inhalation sollte das Opfer in einem gut belüfteten Bereich stehen dürfen. Wenn die Inhalation ernst ist, muss das Opfer so bald wie möglich in einen sicheren Bereich evakuiert werden. Lose enge Kleidung wie Hemdhals, Gürtel oder Krawatte.
Wenn das Opfer schwer zu atmen ist, muss Sauerstoff verabreicht werden. Wenn das Opfer nicht atmet, wird eine Wiederbelebung der Mundmund gemacht. Immer berücksichtigt, dass es für die Person gefährlich sein kann, die Hilfe bietet, die Hilfe für die Wiederbelebung des Mundes anbieten, wenn das inhalierte Material giftig, infektiös oder korrosiv ist.
Es kann Ihnen dienen: Hypophysensäure (H3PO2): Eigenschaften, Verwendung und ReagenzienIn allen Fällen sollte sofortige medizinische Versorgung gesucht werden.
Andererseits ist die Luftverschmutzung aufgrund von Schwefeloxiden ein wichtiges Umweltproblem, wobei jedes Jahr Millionen von Tonnen Schwefeldioxid und Trioxid in die Atmosphäre emittiert werden. Diese Verbindungen sind sowohl für Pflanzen- und Tierleben als auch für viele Baumaterialien schädlich.
Ein weiteres großes Problem ist saurer Regen. Beide Schwefeloxide lösen sich in atmosphärischen Wassertropfen auf, um saure Lösungen zu bilden, was sehr schädlich sein kann, wenn sie in Form von Regen fallen.
Saurer Regen kann Wälder beschädigen und in vielen Seen Fische sterben lassen. Es ist auch korrosiv für Metalle, Kalkstein und andere Materialien. Die möglichen Lösungen für dieses Problem sind aufgrund der Schwierigkeit, den Schwefelschwefel aus Kohle und Öl zu beseitigen, bevor sie verbrennen.
Anwendungen
- Schwefeltrioxid ist ein wesentliches Reagenz bei Sulfonierungsreaktionen. Diese Prozesse bieten Waschmittel, Farbstoffe und Pharmazeutische Produkte. Es wird in situ aus Schwefelsäure erzeugt oder als Raucherschwefelsäurelösung verwendet.
- Seine Desinfektionseigenschaften sind für Jahrhunderte verantwortlich, um die Weinwürfel zu desinfizieren und Schwefel in sich zu verbrennen.
Verweise
- Trioxidschwefel. Von EBI geborgen.AC.Vereinigtes Königreich
- Sicherheitsdatenblatt Schwefeltrioxid. Von Sciencelab geborgen.com

