Chromoxid (III) Struktur, Nomenklatur, Eigenschaften, verwendet

- 1624
- 373
- Joe Hartwig
Er Chromoxid (III) U -Chromoxid ist ein anorganischer grüner Feststoff, der durch Verbrennen von Chrommetall (CR) in Sauerstoff gebildet wird (OR)2), Chrom mit Oxidationszustand 3 lassen 3+. Seine chemische Formel ist Cr2ENTWEDER3. In der Natur ist es im Eskolaíta -Mineral zu finden. Natürliche Ablagerungen von Chromoxid (III) sind nicht bekannt.
Es kann unter anderem durch Erhitzen von CR zubereitet werden2ENTWEDER3 hydratisiert (Cr2ENTWEDER3.NH2O) Wasser vollständig entfernen. Es wird auch als Produkt der Chromoxid -Kalzinierung (VI) (CRO) erhalten3).
 Chromoxidpigment (III). FK1954 [Public Domain]. Quelle: Wikipedia Commons
Chromoxidpigment (III). FK1954 [Public Domain]. Quelle: Wikipedia Commons Der beste Weg, es rein zu erhalten4)2Cr2ENTWEDER7 bei 200 ºC. Industriell wird durch Reduktion von Natriumdichromat (NA) erzeugt2Cr2ENTWEDER7) fest mit Schwefel.
Wenn es fein geteilt ist, zeigt es eine hellgrüne Farbe mit gelblicher Nuance. Aber wenn die Partikel größer sind, zeigt es einen bläulichen Farbstoff. Chromoxid ist das stabilste grüne Pigment, das bekannt ist. Sein thermischer und chemischer Widerstand macht es zu einem wertvollen Keramikfarbstoff.
Es wird in Industriebeschichtungen, Lacken, in der Bauindustrie, in Schmuck, als Färbung in Kosmetika oder in pharmazeutischen Produkten verwendet.
[TOC]
Struktur
Α-CRoxid2ENTWEDER3 Es hat die Struktur vom Typ Corindon. Sein kristallines System ist rhomboonisches sechseckiges Rhomboic. Ist isomorph mit α-Alumina und α-FE2ENTWEDER3.
Das Eskolaíta, natürliches Mineral von Chromoxid (III), zeigt die nachstehend gezeigte Struktur:
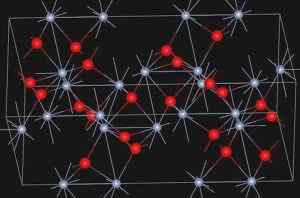 Kristallstruktur von Eskolaíta Mineral. https: // hochladen.Wikimedia.org/wikipedia/commons/e/ee/eskolaite_structure.JPG. Quelle: Wikipedia Commons
Kristallstruktur von Eskolaíta Mineral. https: // hochladen.Wikimedia.org/wikipedia/commons/e/ee/eskolaite_structure.JPG. Quelle: Wikipedia Commons Nomenklatur
- Chromoxid (III).
- Grünes Chromoxid.
- Dichroma -Trioxid.
- Chromseasquioxid.
- Chromie.
- Eskolaíta: Chromoxidmineral (III).
- Hydrat: Cr2ENTWEDER3.NH2Oder (wo n ≅ 2) Chromoxidhydrat (III) oder Guignet Green genannt wird.
 Chromoxidhydrat (III). W. Oelen [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikipedia Commons
Chromoxidhydrat (III). W. Oelen [CC BY-SA 3.0 (https: // creativecommons.Org/lizenzen/by-sa/3.0)]]. Quelle: Wikipedia Commons Eigenschaften
Körperlicher Status
Kristalline Feststoff.
Mohs Härte
9 (ihre Kristalle sind extrem hart).
Molekulargewicht
151,99 g/mol.
Kann Ihnen dienen: quaternäre Verbindungen: Merkmale, Schulungen, BeispieleSchmelzpunkt
Schmilzt bei 2435 ° C, aber es beginnt auf 2000 ºC zu verdampfen, um grüne Rauchwolken zu bilden.
Dichte
5,22 g/cm3
Löslichkeit
Wenn es bei hohen Temperaturen erhitzt wurde, ist es in Wasser praktisch unlöslich (3 Mikrogramm/l bei 20 ° C); unlöslich in Alkoholen und Aceton; leicht löslich in Säuren und Alkalien; Perchlorsäure -Ssolulble (HCLO4) bis 70%, in denen es zusammenbricht.
pH
6.
Brechungsindex
2.551.
Andere Eigenschaften
- Wenn es stark kalkiniert ist, wird es in der Inert zu Säuren und Basen inert. Ansonsten die Cr2ENTWEDER3 und seine hydratisierte Form cr2ENTWEDER3.NH2O Sie sind amphotere und lösten sich in Säure leicht auf, um Aqua- und H (H) zu ergeben2ENTWEDER)6]3+, und in konzentrierten Alkali zur Bildung von "Chromitos".
- Wenn es kalkiniert wurde, ist es chemisch resistent gegen Säuren, Alkalien und hohe Temperaturen. Ist extrem stabil für so2.
- Es hat eine hervorragende Lichtwiderstand.
- Es ist ein extrem hartes Material, Sie können Quarz, Tapacio und Zirkonio kratzen.
- Seine Hydrat -Cr2ENTWEDER3.NH2Oder (wo n ≅ 2) keine thermische Stabilität aufweist, sein Hydratationswasser begrenzt seine Anwendbarkeit auf weniger als 260 ° C. Es präsentiert eine niedrige Färbungskapazität und eine begrenzte Nuance von Nuancen.
- Aber dieses Hydrat hat einen sehr sauberen und hellgrün blauen Farbton. Es ist halbtransparent, bietet eine geringe Deckkraft, eine hervorragende Resistenz gegen Licht und Widerstand gegen Alkalis.
- Die Cr2ENTWEDER3 Es wird nicht als gefährliches Material eingestuft und gilt als träge feines Pulver. Es unterliegt nicht internationalen Verkehrsvorschriften.
- Reiziert weder die Haut noch die Schleimhäute.
Anwendungen
In der Keramik- und Glasindustrie
Aufgrund seiner hohen Resistenz gegen Wärme und chemischer Resistenz die CR2ENTWEDER3 Kalkiniert wird als Farbfärbung oder Fachpigment in der Keramikherstellung, in Porzellan -Emails und Mischungen für Glas.
In Industriebeschichtungen
Keramik mit Chromoxid (III) bietet eine hervorragende Resistenz gegen die meisten korrosiven Umgebungen. All dies durch den Mechanismus des Ausschlusses des umgebenden Substrats.
Aus diesem Grund wird es in Beschichtungen verwendet, um die Korrosion vieler Materialien zu verhindern, die durch Wärmespray angewendet werden (Zerstäubung oder heißer Tau).
Kann Ihnen dienen: Chemischer Prozess: Prinzipien, Typen, BeispieleEs wird auch als Schutz vor abrasiven Verschleiß verwendet (wenn die Entfernung des Materials durch Partikel verursacht wird, die sich durch eine Oberfläche bewegen).
In diesen Fällen die Anwendung einer CR -Beschichtung2ENTWEDER3 Durch Ablagerung mit Plasma erzeugt es eine hohe Abriebfestigkeit.
Die beiden vorherigen Fälle haben beispielsweise Nützlichkeit in Gas -turlocial Turbinenmotoren.
In der feuerfestigen Industrie
Es wird in thermisch und chemisch resistenten Ziegeln, Beschichtmaterialien und auf Aluminiumoxid basierender refraktärer Beton verwendet.
Im Aufbau
Da es äußerst resistent gegen atmosphärische Bedingungen, Licht und Wärme ist, wird es als granulierter Gesteinsfarbstoff für Asphaltdächer, Betonzement, hochwertige Industriebeschichtungen für Außenkonstruktionen, Stahlkonstruktionen und Fassadenbeschichtung (emulsionierbare Farben) aufgetragen (emulsionierbare Farben).
Als Pigment in verschiedenen Anwendungen
Es kann Vulkanisierungsbedingungen unterstützen und sich nicht verschlechtert, daher wird es bei der Gummipigmentierung verwendet.
Weil sie nicht technisch sind.
In der Pigmentindustrie wird es als Rohstoff verwendet, um durchdringende Farbstoffe zu produzieren, die Chrom und Pigmente basieren, die auf Phasen von gemischten Metalloxiden basieren. Es wird auch als Färbung von Gemälden für die Spulenbeschichtung verwendet.
Sein Hydrat hat eine Transparenz, die die Formulierung polychromatischer Oberflächen in der Automobilindustrie ermöglicht (metallische Auto -Oberflächen).
Aufgrund seines einzigartigen Merkmals für die Reflexion von Infrarotstrahlung (IR) ähnlich wie bei Pflanzen Chlorophyll, scheint es bei Infrarotlicht Laub zu sein. Aus diesem Grund ist die Verwendung in Tarnbilder oder Beschichtungen für militärische Anwendungen sehr weit verbreitet.
Im Schmuck
Es wird als Farbstoff synthetischer Edelsteine verwendet. Wenn CR eingeführt wird2ENTWEDER3 als Verunreinigung im kristallinen Netzwerk von α-al2ENTWEDER3, Wie im semi-preziösen Rubinmineral ist die Farbe rot statt grün.
Es wird auch als Schleifmittel verwendet und für hohe Härte und Schleifeigenschaften poliert.
Auf chemische Reaktionen
In Alumina unterstützt (zu2ENTWEDER3) oder andere Oxide werden in der organischen Chemie als Katalysator verwendet, beispielsweise bei der Hydrierung von Estern oder Aldehyden zur Bildung von Alkoholen und in der Kohlenwasserstoffzyklierung. Katalysiert die Reaktion von Stickstoff (n2) mit Wasserstoff (h2) Ammoniak (NH3).
Es kann Ihnen dienen: Lithium: Geschichte, Struktur, Eigenschaften, Risiken und VerwendungFür seine Oxid-Reduktionskapazität spielt zusammen mit Chromoxid (VI) eine wichtige Rolle bei der Dehydrierung von Alkanen2 Propeno und Isobuten produzieren, da der Katalysator-Deaktivierungsreaktivierungszyklus leicht ausführbar ist. Es wird auch als Katalysator in der anorganischen Chemie verwendet.
In der Chromherstellung
Es wird in der reinen Chrommetall -Aluminothermie verwendet. Dazu muss es auf 1000 ° C erhitzt werden, um seine Korngröße zu erhöhen.
 Chrommetallpräparation durch aluminotherme Reduktion von Chromoxid (III). Rando Tuiken [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikipedia Commons
Chrommetallpräparation durch aluminotherme Reduktion von Chromoxid (III). Rando Tuiken [CC BY-SA 4.0 (https: // creativecommons.Org/lizenzen/by-sa/4.0)]]. Quelle: Wikipedia Commons In magnetischen Materialien
Es wurde in kleinen Mengen zu magnetischen Materialien von Audio- und Videobändern hinzugefügt, indem er solide Köpfe selbst immateriell verehrt wird.
Jüngste Innovationen
Es wurden Pigmente erhalten, die das Reflexionsvermögen von nahezu Dopar CR -Nanopartikeln verbessert haben2ENTWEDER3 mit Salzen von Elementen, die zur Seltenerdgruppe gehören, wie dem Lantano und dem Praseodimio.
Wenn die Konzentration dieser Elemente erhöht wird, nimmt das Sonnenreflexion des nahezu Infrarots zu, ohne die grüne Farbe des Cr -Schweins zu beeinflussen2ENTWEDER3.
Dies ermöglicht die Klassifizierung von CR2ENTWEDER3 Doping als "kaltes" Pigment, da es zur Kontrolle der Wärmeakkumulation geeignet ist.
Auf Decken, Autos und Polsterung wird unter anderem ein hohes Reflexionsvermögen des IR -Sonnenlicht.
Verweise
- Baumwolle, f. Albert und Wilkinson, Geoffrey. (1980). Fortgeschrittene anorganische Chemie. Vierte Edition. John Wiley & Söhne.
- Kirk-Othmer (1994). Enzyklopädie der chemischen Technologie. Band 19. Vierte Edition. John Wiley & Söhne.
- Ullmanns Enzyklopädie der industriellen Chemie. (1990). FÜNFTE AUSGABE. Band A7 und A20. VCH Verlagsgellschaft MBH.
- Amerikanische Elemente. (2019). Chrom (III) Oxid. Von Amerikanern erholt.com.
- Nationalbibliothek für Medizin. (2019). Chrom (III) Oxid. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung.
- Dorfman, Mitchell R. (2012). Wärmesprühbeschichtungen. Im Handbuch zur Umweltverschlechterung von Materialien. Kapitel 19. Von Scientedirect erholt.com.
- Takehira, k. et al. (2004). CO2 Dehydrierung von Propan über CR-MCM-41-Katalysator. In Studien in Oberflächenwissenschaft und Katalyse 153. Von Scientedirect erholt.com.
- Selvam Sangeetha et al. (2012). Funktionelle Pigmente aus Chrom (III) Nanopartikeloxid. Farbstoffe und Pigmente 94 (2012) 548-552. Von Scientedirect erholt.com.
- « Geschichte und bedeutungsvoller Schild in der VAIen
- Titangeschichte, Struktur, Eigenschaften, Reaktionen, verwendet, verwendet »

