Grundoxide

- 2740
- 31
- Ibrahim Steuk
Wir erklären, was die Grundoxide sind, wie ihre Eigenschaften, ihre Nomenklatur und einige Beispiele gebildet werden
 Viele grundlegende Oxide haben auffällige, charakteristisch für Metallfarben
Viele grundlegende Oxide haben auffällige, charakteristisch für Metallfarben Was sind grundlegende Oxide?
Der Grundoxide Sie sind anorganische Verbindungen, die durch die Vereinigung zwischen Sauerstoff und Metall gebildet werden. Sie werden als Basixide bezeichnet, weil sie beim Auflösen in Wasser alkalische oder grundlegende Lösungen produzieren. Auch weil sie mit Säuren reagieren, um durch eine Säure-Base-Neutralisationsreaktion ein Salz und Wasser zu bilden.
Grundoxide sind sehr häufig. Tatsächlich sind die meisten Metalle in der Natur in Oxides -Böden vorhanden, so dass sie früher Land bezeichnet wurden.
Grundoxide sind für die Branche von großer Bedeutung. Viele in der Branche verwendete farbige Pigmente sind Oxide. Andere Oxide werden als Basis für Gemälde verwendet, insbesondere für Titan-, Blei- und Zinkoxide.
Grundlegende Oxide Eigenschaften
Sie sind binäre Verbindungen
Diese Verbindungen werden nur durch zwei Elemente gebildet: Sauerstoff und ein Metall. Daher sind sie binäre Verbindungen.
Seine empirische Formel ist m2ENTWEDERX oder moX/2
Die Valenz von Sauerstoff in Oxiden beträgt immer -2. Das Gleiche geschieht jedoch nicht, wenn es seltsam ist.
Zum Beispiel ist die empirische Formel von Natriumoxid na2Oder weil das Natrium Valencia +1 hat (ungerade). Stattdessen ist die empirische Formel von Calciumoxid CAO, da Calcium Valencia +2 hat.
Sie sind anorganische Verbindungen, fast immer ionisch
Die meisten grundlegenden Oxide sind kristalline ionische Verbindungen. Dies schließt die Oxide aller alkalischen Metalle aller Alkaliner (außer Beryllium) und die erste Reihe von Übergangsmetallen ein.
Kann Ihnen dienen: Chemische BindungSie haben sehr hohe Fusion- und Siedepunkte
Die ionische Bindung hält alle Ionen, die grundlegende Oxide bilden. Dies macht es schwierig zu schmelzen und noch schwieriger zu verdampfen. Aus diesem Grund haben sie sehr hohe Fusions- und Siedepunkte.
Sie sind bei Raumtemperatur solide
Aufgrund der gleichen Tatsache wie hohe Fusionspunkte sind alle grundlegenden Oxide bei Raumtemperatur fest.
Sie sind Grundverbindungen
Der Grund, warum sie Basisoxide genannt werden. Oxide mit größeren ionischen Charakteren erzeugen Basislösungen beim Auflösen in Wasser und reagieren auch mit Säuren, um sie neutralisieren.
Es ist jedoch zu beachten, dass nicht alle Metalloxide grundlegend sind. Einige sind neutral, andere Säuren und andere Amphotor.
Die meisten sind wenig löslich oder unlöslich im Wasser
Alle Grundoxide sind in Wasser unlöslich, mit Ausnahme von alkalischen und Bariummetallenoxiden. Sie sind jedoch in Säurelösungen löslich.
Wie sind Grundoxide?
Grundoxide können spontan gebildet werden, wenn Metalle Luftsauerstoff ausgesetzt sind. Tatsächlich bestehen Korrosionsschichten, die auf der Oberfläche von Metallen gebildet werden.
Das Metall betrifft im Allgemeinen ist es ein alkalisches, alkalisches Metall oder ein Übergangsmetall.
Sie können drei allgemeine Reaktionen für die Bildung von Oxiden schreiben, je nachdem, ob die Metallvalencia gerade oder ungerade ist:
Für Metalle mit seltsamen Valences:
Wenn das Metall eine seltsame Valenz hat, ist die allgemeine Reaktion der Oxidbildung:

Zum Beispiel ist die Reaktion zur Bildung von Natriumoxid, wobei Natrium Valencia +1 hat,:
Es kann Ihnen dienen: Phosphor: Anamnese, Eigenschaften, Struktur, Erhalten, Verwendungen
Ein weiteres Beispiel ist die Bildung von Eisenoxid, bei dem Eisen Oxidation oder Valencia +3 aufweist. In diesem Fall lautet die Reaktion:

Für Metalle mit Valencia +2:
Wenn das Metall Valencia +2 hat, lautet die allgemeine Reaktion der Oxidbildung:

Beispielsweise ist bei Calciumoxidbildung, wobei Calcium Valencia +2 hat, die Reaktion:

Für Metalle mit anderen Paaren:
Wenn das Metall zusätzlich zu +2 auch Valences hat, ist die allgemeine Reaktion der Oxidbildung:
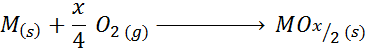
Ein Beispiel für diesen Fall ist die Titanoxid -Bildungsreaktion (IV):

Grundlegende Oxid -Nomenklatur
Es gibt drei Nomenklatursysteme für die grundlegenden Oxide: die traditionelle Nomenklatur, die Aktie und die systematische.
Um ein Oxid gemäß den ersten beiden Nomenklatursystemen zu benennen.
Traditionelle Nomenklatur
Nach der traditionellen Nomenklatur werden grundlegende Oxide beginnend mit dem Wort benannt entwederXido gefolgt vom Kationennamen. Dieser Nachname wird erstellt, indem die Wurzel des Metallnamens und ein System von Präfixen und Suffixen platziert wird, die durch die Metall Valencia angegeben sind:
Oxid + Präfix-raí-sufijo
Die Regeln für die Zuweisung von Präfixen und Suffixen sind in der folgenden Tabelle zusammengefasst:
Anzahl möglicher Valences | Valencia | Präfix | Suffix |
1 einzelne Valencia | |||
Nur | --- | ___ICO | |
2 Valencias | |||
Alten | --- | ___ICO | |
Unerheblich | --- | ___tragen | |
3 Valences | |||
Alten | --- | ___ICO | |
Dazwischenliegend | --- | ___tragen | |
Unerheblich | Schluckauf___ | ___tragen | |
4 Valences | |||
Alten | Pro___ | ___ICO | |
Hauptvermediat | --- | ___ICO | |
Geringfügige Zwischenprodukt | --- | ___ICO | |
Unerheblich | Schluckauf___ | ___ICO |
Beispiel:
Er Glaube2ENTWEDER3 Es ist ein Eisenoxid mit Valencia +3. Iron hat nur zwei Valenzen, die +2 und +3 sind. In diesem Oxid hat das Eisen das älteste von zwei Valenzen. Aus diesem Grund wird das Suffix hinzugefügt ___ICO an der Wurzel des Namens des Eisenmetalls, der ist Ferr-.
Es kann Ihnen dienen: keine Elektrolyte: Eigenschaften und BeispieleDaher der traditionelle Name von Glaube2ENTWEDER3 Ist: Eisenoxid.
Stock Nomenklatur
In diesem System wird der Name beginnend mit den Wörtern erstellt Oxid von, gefolgt von Metallname. Schließlich wird seine Valencia in Römer in Klammern untergebracht:
Metall + Name Oxid (Valencia)
Wenn das Metall nur eine Valenz hat, wird es weggelassen.
Beispiel:
In Cr2ENTWEDER3 Chrom hat Valencia +3, also ist der Namensbestand Chromoxid (III).
Systematische Nomenklatur
Dies ist die einzige der drei Nomenklaturen, die das Metall Valencia nicht angeben. Sitematische Namen geben an, wie viele Sauerstoff- und Metallatome die Verbindung unter Verwendung numerischer Präfixe enthalten.
Der Name wird mit dem Wort erstellt Oxid Vor ihm Präfix, der die Anzahl der Sauerstoff angibt, Dann der Artikel von gefolgt von Metallname mit seinem jeweiligen Präfix.
Präfix-Oxid + des + Präfix-Metalls
Einige Präfixe sind:
Nummer | Präfix |
1 | Brötchen |
2 | Gab |
3 | Tri |
4 | Tetra |
5 | Penta .. |
Beispiel:
In der systematischen Nomenklatur die Cr2ENTWEDER3 Es heißt Dichroma -Trioxid, da es drei Sauerstoff und zwei Chromos hat.
Beispiele für Grundoxide
- Natriumoxid - Na2ENTWEDER
- Eisenoxid - Glaube2ENTWEDER3
- Eisenmonoxid - hässlich
- Cromicoxid - Cr2ENTWEDER3
- Divanadio Pentaoxid - V2ENTWEDER5
- Kaliumoxid - k2ENTWEDER
- Bariumoxid - Bao

